题目内容
20.乳酸在一定条件下所形成的聚酯的结构简式为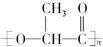 ,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )
,该酯可以作为新型的餐具原料.由它所产生的塑料在乳酸菌作用下,能迅速分解为无毒物质,可以降解.下列有关这种新型的可降解塑料的叙述正确的是( )| A. | 降解塑料是一种纯净物 | |
| B. | 其生产过程中的聚合方式与聚苯乙烯相似 | |
| C. | 它属于一种线型高分子材料 | |
| D. | 其相对分子质量为72 |
分析 A.降解塑料为高聚物,n值不确定,是一种混合物;
B.聚乳酸发生缩聚反应生成,而聚苯乙烯为加聚产物;
C.线型高分子材料具有热塑性;
D.其相对分子质量为括号内的分子量乘以n.
解答 解:A.该降解塑料是乳酸在一定条件下的聚合产物,其聚合度n值是不确定的,它是相对分子质量大小不等的混合物,故A错误;
B.由乳酸生成其聚酯属于缩聚反应,它的链节彼此连接在一起形成一条长链,属于一种线型高分子化合物,而苯乙烯生成聚苯乙烯发生的则是加聚反应,故B错误;
C.塑料都有热塑性,故其属于线型高分子材料,故C正确;
D.该聚合物的相对分子质量为72n,故D错误;
故选C.
点评 本题主要考查对高分子化合物的理解,题目难度不大,注意高聚物与单体的联系与区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.初中常见的3种元素X、Y和Z的相关信息如下表所示.
请用元素符号或化学式回答下列问题:
(1)Z的元素符号是O.
(2)X的元素原子容易变成X+,其原因是金属性强.
(3)Y的单质与不充足的Z的单质反应,其产物的化学式为CO.
(4)YZ2可与X的氢氧化物发生反应,该反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
(5)由X、Y、Z三种元素组成的化合物与一定量的稀盐酸混合后的现象为有气体生成,该反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.
| 元素 | X | Y | Z |
| 相关 信息 | 食盐中存在的 金属元素 | 其一种单质是天然 存在的最硬的物质 | 地壳中含量 最多的元素 |
(1)Z的元素符号是O.
(2)X的元素原子容易变成X+,其原因是金属性强.
(3)Y的单质与不充足的Z的单质反应,其产物的化学式为CO.
(4)YZ2可与X的氢氧化物发生反应,该反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
(5)由X、Y、Z三种元素组成的化合物与一定量的稀盐酸混合后的现象为有气体生成,该反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.
8.下列反应的离子方程式正确的是( )
| A. | 碳酸钙溶于醋酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯化铁溶液溶解铜 Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 氯气溶于水 Cl2+H2O═2H++Cl-+ClO- | |
| D. | 氢氧化钠溶液吸收二氧化硫气体 SO2+2OH-═SO42-+H2O |
5.下列各组中两种溶液间的反应,均可用同一离子方程式表示的是( )
| A. | CH3COOH和Na2CO3与CH3COOH和NaHCO3 | |
| B. | AgNO3和HCl与AgNO3和NaCl | |
| C. | BaCl2和Na2SO4 与Ba(OH)2和H2SO4 | |
| D. | KOH和AlCl3与氨水和AlBr3 |
12.某溶液中有:①Cu2+、②NH4+、③Fe2+、④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再向其中加入过量盐酸,溶液中大量减少的阳离子是( )
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
9.向一定量的 Fe、FeO 和 Fe2O3的混合物中加入 150mL 4mol/L 的稀硝酸,恰好使混合物 完全溶解,放出 1.792L NO(标准状况),往所得溶液中加入 NH4SCN 溶液,无红色出现.若 用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
| A. | 0.26mol | B. | 0.28 mol | C. | 0.30 mol | D. | 0.32 mol |
10.能把稀硫酸、氢氧化钠和氯化钠三种溶液一次性鉴别出来的试剂是( )
| A. | 紫色石蕊溶液 | B. | 无色酚酞溶液 | C. | 碳酸钠溶液 | D. | 硝酸钾溶液 |
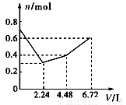
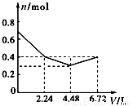
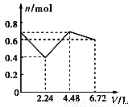
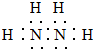 ,其中氮的化合价为-2价.
,其中氮的化合价为-2价.