题目内容
13.常温下,下列有关溶液中微粒的物质的量浓度关系不正确的是( )| A. | 向0.1mol/LpH=2的HF溶液加水稀释,$\frac{c({H}^{+})}{c(HF)}$增大 | |
| B. | 向0.2 mol/L NaHCO3溶液中加入等体积0.1 mol/L NaOH溶液c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| C. | 向0.1mol/L NaHSO3溶液中通入NH3至中性(溶液体积视为不变),则 c(NH4+)+c(H2SO3)═c(SO32-) | |
| D. | 现有常温下水电离出的c(H+)均为1×10-11 mol/L且体积相同的三种溶液:①HCl溶液②CH3COOH溶液③NaOH溶液,分别与足量铝粉反应,生成氢气的量③最少 |
分析 A.HF属于弱电解质,加水不断稀释时,电离程度增大,平衡常数不变;
B.向0.2 mol/L NaHCO3溶液中加入等体积0.1 mol/L NaOH溶液,发生:HCO3-+OH-=CO32-+H2O,反应后溶液中存在等量的HCO3-和CO32-,且二者都水解,溶液呈碱性;
C.溶液中存在电荷守恒和物料守恒计算分析判断;
D.常温下水电离出的c(H+)均为1×10-11mol/L,则溶质抑制了水的电离,该溶液为酸溶液或碱溶液,①③为强电解质,都是一元强酸或强碱,则二者浓度为0.001mol/L;②为弱电解质,在溶液中只能部分电离,则其浓度大于0.001mol/L,铝足量,酸、碱溶液完全反应,根据浓度大小及氢离子、氢氧根离子与生成氢气的量的关系判断;
解答 解:A.因Ka(HF)=$\frac{c({H}^{+})c({F}^{-})}{c(HF)}$,当HF溶液加水不断稀释,促进电离,c(H+)不断减小,温度不变,Ka(HF)不变,所以$\frac{c({H}^{+})}{c(HF)}$增大,故A正确;
B.向0.2mol/L的NaHCO3溶液中加入等体积0.1mol/LNaOH溶液,发生:HCO3-+OH-=CO32-+H2O,反应后溶液中存在等量的HCO3-和CO32-,因CO32-水解程度大于HCO3-,则c(Na+)>c(HCO3-)>c(CO32-),溶液呈碱性,c(OH-)>c(H+),因水解程度较小,则c(CO32-)>c(OH-),所以离子浓度大小顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故B正确;
C.溶液中电荷守恒c(Na+)+c(H+)+c(NH4+)=c(OH-)+c(HSO3-)+c(SO32-),物料守恒c(Na+)=c(HSO3-)+c(SO32-)+c(H2SO3),向0.1mol/L NaHSO3溶液中通入NH3至中性,c(H+)=c(OH-),得到 c(NH4+)+c(H2SO3)═c(SO32-),故C正确;
D.常温下水电离出的c(H+)均为1×10-11mol/L,则溶质抑制了水的电离,该溶液为酸溶液或碱溶液,①③为一元强酸或强碱,则二者浓度为0.001mol/L;②为弱电解质,在溶液中只能部分电离,则其浓度大于0.001mol/L,铝足量时,2mol氯化氢生成1mol氢气,2mol氢氧化钠生成3mol氢气,①③的浓度相等,所以③生成的氢气大于①;②的浓度大于①,所以生成的氢气大于①,即:等体积、铝足量时①生成的氢气最少,故D错误;
故选D.
点评 本题考查了弱电解质的电离及其影响、电解质溶液中电荷守恒、物料守恒的分析,题目难度中等,明确酸碱溶液对水的电离的影响为解答关键,注意明确弱电解质在溶液中部分电离,试题侧重考查学生的分析、理解能力.

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案| A. | 原子总数 | B. | 质子总数 | C. | 电子总数 | D. | 质量 |
| A. | 氟化氢的电子式: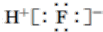 | B. | 中子数为21的钾原子:${\;}_{19}^{40}$K | ||
| C. | NH3的结构式: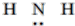 | D. | N3-的结构示意图: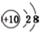 |
| A. | 酸与醇反应一定能生成酯,且酯化反应是可逆反应 | |
| B. | CO2通入饱和苯酚钠溶液,用分液法可以得到苯酚 | |
| C. | 有机物 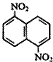 的n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6 的n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6 | |
| D. | 等物质的量的烃或烃的含氧衍生物A和B完全燃烧时,消耗氧气的量相等.则A和B的分子量相差可能为18n或44n(n为正整数) |
| A. | 向饱和碳酸氢钙溶液中加入过量的NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| B. | KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀:2Al3++3 SO42-+3 Ba2++6 OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O | |
| D. | 硫酸亚铁加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++4H2O |

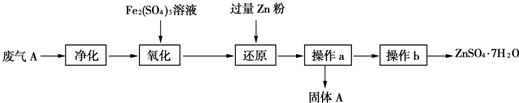
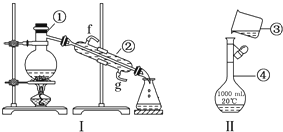
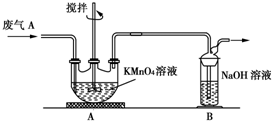 ①为了保证实验成功,装置A应具有的现象是KMnO4溶液的紫红色不能完全褪色,搅拌的目的是提高SO2的吸收率.
①为了保证实验成功,装置A应具有的现象是KMnO4溶液的紫红色不能完全褪色,搅拌的目的是提高SO2的吸收率.