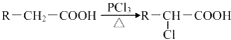题目内容
16.准确移取20.00mL某待测HCl溶液于锥形瓶中,用0.1000mol•L-1NaOH溶液滴定,测HCl溶液的浓度,下列操作中正确的是( )| A. | 锥形瓶用蒸馏水洗涤后,用待测HCl溶液润洗 | |
| B. | 滴定管用蒸馏水洗涤后,直接装入NaOH溶液进行滴定 | |
| C. | 滴定时,没有逐出滴定管下口的气泡 | |
| D. | 读数时,视线与滴定管内液体的凹液面最低处保持相平 |
分析 A.锥形瓶不能润洗,否则会导致待测液中氯化氢的物质的量偏大;
B.滴定管必须润洗,否则会导致标准液浓度减小,测定结果偏高;
C.滴定管中有气泡,影响了标准液体积;
D.读数时,视线应该与滴定管内凹液面最低处相平.
解答 解:A.锥形瓶用蒸馏水洗涤后,不能润洗,如果用待测HCl溶液润洗后,滴定过程中导致消耗标准液体积偏大,测定结果偏高,故A错误;
B.滴定管用蒸馏水洗涤后,直接装入NaOH溶液进行滴定,导致标准液被稀释,则滴定过程中消耗标准液体积偏大,测定结果偏高,故B错误;
C.滴定时必须赶出滴定管中气泡,否则会影响测定结果,故C错误;
D.读数时,视线应该与滴定管内液体的凹液面最低处保持相平,该操作方法合理,故D正确;
故选D.
点评 本题考查了中和滴定的操作方法,题目难度不大,明确中和滴定操作方法为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
1.25℃时,用0.1mol•L-1的NaOH溶液滴定0.1mol•L-1CH3COOH(Ka=1.75×10-5)溶液过程中,消耗NaOH溶液的体积与溶液pH的关系如图所示,下列各项中微粒浓度间关系正确的是( )

| A. | 点①所示溶液中:2c(CH3COO-)-2c(CH3COOH)=c(H+)-c(OH-) | |
| B. | 点②所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| C. | 点③所示溶液中:c(CH3COO-)-c(CH3COOH)=c(Na+)+2c(H+)-2c(OH-) | |
| D. | pH=12的溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)>c(CH3COOH) |
4.实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏高的是( )
| A. | 酸式滴定管在装酸液前用标准盐酸溶液润洗2~3次 | |
| B. | 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 | |
| C. | 锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 | |
| D. | 盛NaOH溶液的锥形瓶滴定前未用NaOH溶液润洗 |
11.在25℃时,pH等于11的NaOH溶液和NaCN溶液中,水的电离度大小的比较正确的是( )
| A. | 两者相等 | B. | 前者比后者大11倍 | ||
| C. | 后者是前者的108倍 | D. | 后者是前者的1011倍 |
1.[探究实验一]某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见表,表中的“实验方案”与“实验现象”前后不一定是对应关系):
请你帮助该同学整理并完成实验报告.
(1)实验目的:探究同周期主族元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的强弱,请你设计实验(实验用品自选,不要求写化学方程式):向溶液中滴加NaOH溶液至过量,得白色沉淀,不溶解;向溶液中滴加NaOH溶液至过量,产生白色胶状沉淀,继而沉淀消失;
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强;
[探究实验二]一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂.为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
(注:催化效果用单位时间内每克催化剂得到产品的质量来表示)
(6)表中ω=74.45;
(7)从实验1、2可以得出的结论是:氯化镁固体含水量越高,催化剂催化效果越差是:..
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
(1)实验目的:探究同周期主族元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强;
[探究实验二]一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂.为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
| 实验 序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式/ | 催化效果/g•g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 | ω | 100 | 振动球磨 |
(6)表中ω=74.45;
(7)从实验1、2可以得出的结论是:氯化镁固体含水量越高,催化剂催化效果越差是:..
8.下列各项中不属于化学科学研究内容的是( )
| A. | 寻找性能良好的新材料 | B. | 治理环境污染 | ||
| C. | 开发新能源 | D. | 研究质子、中子的结构 |
5.空气质量报告的各项指标可以反映出各地空气的质量.下列气体已纳入我国空气质量报告的是( )
| A. | CO2 | B. | N2 | C. | NO2 |
6.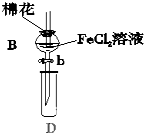 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气.
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子.
Ⅲ.接着再向B中通入一定量的SO2气体.
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子.
(1)棉花中浸润的溶液为NaOH溶液,目的是防止污染环境.
(2)实验室制备氯气的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)过程Ⅲ中一定发生反应的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是取溶液少许于试管中,先加入足量稀盐酸酸化,再滴加少量BaCl2溶液,若有白色沉淀生成,证明有SO42-,反之无SO42-.
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是SO2>Fe2+>Cl-
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是乙、丙.
 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气.
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子.
Ⅲ.接着再向B中通入一定量的SO2气体.
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子.
(1)棉花中浸润的溶液为NaOH溶液,目的是防止污染环境.
(2)实验室制备氯气的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)过程Ⅲ中一定发生反应的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是取溶液少许于试管中,先加入足量稀盐酸酸化,再滴加少量BaCl2溶液,若有白色沉淀生成,证明有SO42-,反之无SO42-.
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是SO2>Fe2+>Cl-
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是乙、丙.
| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |