题目内容
9.下列有关0.1mol/L NaOH溶液的叙述不正确的是( )| A. | 1 L该溶液中含有NaOH 4.0 g | |
| B. | 给NaOH溶液通电,使NaOH发生电离 | |
| C. | NaOH的电离方程式是:NaOH═Na++OH- | |
| D. | NaOH溶液能导电,是因为溶液中有自由移动的Na+、OH-离子 |
分析 A.根据n=cV计算氢氧化钠物质的量,再根据m=nM计算其质量;
B.氢氧化钠的电离,是在水中,不需要通电;
C.氢氧化钠是强电解质,属于强碱,能完全电离出钠离子和氢氧根离子;
D.溶液导电的原因是溶液中存在自由移动离子.
解答 解:A.0.1L溶液中氢氧化钠物质的量为0.1L×0.1mol/L=0.01mol,其质量为0.01mol×40g/mol=0.4g,故A正确;
B.氢氧化钠在水溶液中能发生电离,条件不是通电,故B错误;
C.氢氧化钠完全电离出钠离子和氢氧根离子,故C正确;
D.氢氧化钠能导电,是由于氢氧化钠在水中电离出钠离子和氢氧根离子,故D正确,
故选B.
点评 本题主要考查的是氢氧化钠溶液的概念以及氢氧化钠的电离,本题难度不大,掌握物质的量的有关公式是关键.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
19.下列各组物质或概念中,在物质分类里,前者不从属于后者的一组是( )
| A. | 空气,分散系 | B. | 电解质,化合物 | C. | 酸,化合物 | D. | 金属,氧化物 |
20.某化学小组同学用下列装置(气密性已检验)进行实验.

(1)探究O2与KI溶液发生反应的条件.
①甲、乙两同学选用以下试剂进行实验(0.1mol•L-1 KI溶液,30% H2O2溶液、0.1mol•L-1H2SO4溶液、淀粉溶液、MnO2固体、KMnO4固体),实验记录如下.
甲制取O2的化学方程式是2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.乙实验中O2与KI溶液反应的离子方程式是O2+4I-+4H+=2I2+2H2O.
②甲用Ⅱ加入试剂替换Ⅰ后,Ⅳ中仍加入KI、淀粉溶液,再次实验时Ⅳ中溶液不变蓝.由此他猜测第一次实验时可能是Ⅰ中的白雾使溶液变蓝.甲又将Ⅰ中产生的气体直接通入下列a溶液(填序号),证明了白雾中含有H2O2.
a.酸性KMnO4 b.FeCl2 c.Na2S
③由甲、乙两同学的实验,可得出结论:KI溶液在酸性条件下易被O2氧化.
(2)资料显示:KI溶液在空气中被缓慢氧化时CO2参与了反应.丙、丁两同学为探究该反应中CO2的作用,进行下列实验.
①丙实验的目的是证明CO2不能氧化I-.
②丁实验的Ⅲ中发生反应方程式为Na2O2.
③为证明CO2所起的作用,可进行的操作是:取上述丁实验后Ⅳ中溶液,滴入CaCl2(或BaCl2)溶液.

(1)探究O2与KI溶液发生反应的条件.
①甲、乙两同学选用以下试剂进行实验(0.1mol•L-1 KI溶液,30% H2O2溶液、0.1mol•L-1H2SO4溶液、淀粉溶液、MnO2固体、KMnO4固体),实验记录如下.
| 操作 | 现象 | |
| 甲 | 向Ⅰ中加入必要的试剂,并向Ⅳ中加入KI、淀粉溶液.连接Ⅰ、Ⅳ,打开活塞 | Ⅰ中剧烈反应,产生无色气体并伴随大量白雾;Ⅳ中有气泡冒出,溶液迅速变蓝 |
| 乙 | 向Ⅱ中加入必要的试剂,并向Ⅳ中加入KI、淀粉溶液和稀硫酸.连接Ⅱ、Ⅳ,点燃酒精灯 | Ⅳ中有气泡冒出,溶液变蓝 |
②甲用Ⅱ加入试剂替换Ⅰ后,Ⅳ中仍加入KI、淀粉溶液,再次实验时Ⅳ中溶液不变蓝.由此他猜测第一次实验时可能是Ⅰ中的白雾使溶液变蓝.甲又将Ⅰ中产生的气体直接通入下列a溶液(填序号),证明了白雾中含有H2O2.
a.酸性KMnO4 b.FeCl2 c.Na2S
③由甲、乙两同学的实验,可得出结论:KI溶液在酸性条件下易被O2氧化.
(2)资料显示:KI溶液在空气中被缓慢氧化时CO2参与了反应.丙、丁两同学为探究该反应中CO2的作用,进行下列实验.
| 操作 | 现象 | |
| 丙 | 向Ⅰ中加入Na2CO3和稀硫酸,Ⅳ中加入KI、淀粉溶液并在上层覆盖少量煤油.使Ⅰ中发生反应将装置中空气排尽后,再将气体通入Ⅳ的溶液中 | Ⅳ中有气泡冒出,溶液不变蓝 |
| 丁 | 向Ⅰ中加入Na2CO3和稀硫酸,Ⅲ中加入必要试剂,Ⅳ中加入KI、淀粉溶液.依次连接Ⅰ、Ⅲ、Ⅳ,打开活塞 | Ⅳ中有气泡冒出,溶液变蓝 |
②丁实验的Ⅲ中发生反应方程式为Na2O2.
③为证明CO2所起的作用,可进行的操作是:取上述丁实验后Ⅳ中溶液,滴入CaCl2(或BaCl2)溶液.
14.在4mol/L的硫酸和2mol/L的硝酸混合溶液10mL中,加入0.96g铜粉,充分反应后,最多可以收集到的标准状况下的气体体积为( )[提示:稀硝酸和铜粉的化学反应为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O].
| A. | 112 mL | B. | 224 mL | C. | 448 mL | D. | 560 mL |
19.下列关于胶体的叙述错误的是( )
| A. | 胶体区别于其它分散系的本质特征是分散质的微粒直径在1nm~100nm之间 | |
| B. | 用平行光照射CuSO4溶液和Fe(OH)3胶体,可以加以区分 | |
| C. | 把FeCl3饱和溶液滴入到NaOH溶液中,以制取Fe(OH)3胶体 | |
| D. | 胶体是一种介稳性的分散系,其粒子能通过滤纸 |

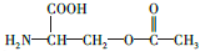 .
. b.在稀硫酸中水解有乙酸生成
b.在稀硫酸中水解有乙酸生成 .
.