题目内容
6.NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 0.1mol的白磷(P4)或CCl4中所含的共价键数均为0.4NA | |
| B. | S2和S8的混合物共6.4g,其中所含的电子数一定为3.2NA | |
| C. | 5.4gAl分别于含溶质0.2mol的NaOH溶液、盐酸反应,生成H2分子数均为0.3NA | |
| D. | 在H2O2+Cl2═2HCl+O2反应中,每生成32gO2,转移4 NA个电子 |
分析 A.白磷分子中含有6个P-P键,CCl4分子中含有4个C-Cl键;
B.S2和S8均由S原子构成,且S原子中含16个电子;
C.求出铝的物质的量,然后根据1molAl~3molHCl,1molAl~1molNaOH来分析;
D.在H2O2+Cl2═2HCl+O2反应中,氯气做氧化剂,生成1mol氧气消耗1mol氯气,生成2mol氯离子,转移2mol电子.
解答 解:A.白磷分子中含有6个P-P键,CCl4分子中含有4个C-Cl键,0.1mol的白磷(P4)共价键数0.6mol,0.1molCCl4中所含的共价键数均为0.4NA,故A错误;
B.S2和S8均由S原子构成,故6.4g混合物中含有的S原子的物质的量为0.2mol,而且S原子中含16个电子,故0.2molS原子中含3.2NA个电子,故B正确;
C.5.4g铝的物质的量为0.2mol,而由于1molAl~3molHCl,1molAl~1molNaOH,故0.2mol铝与0.2mol氢氧化钠能恰好完全反应,而与0.2mol盐酸反应时,铝过量,由于反应掉的铝的物质的量不同,故生成的氢气分子个数不同,故C错误;
D.在H2O2+Cl2═2HCl+O2反应中,氯气做氧化剂,生成1mol氧气消耗1mol氯气,生成2mol氯离子,转移2mol电子,则生成氧气32g,物质的量为1mol,转移2NA个电子,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意白磷与甲烷空间结构、注意过氧化氢中氧元素为-1价,题目难度不大.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
14.短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素同周期;X的金属性在同周期元素中最强;Y原子的电子层数与最外层电子数相等;Z元素在地壳中的含量居于第二位;W的最高价氧化物的水化物的化学式为HnWO2n+2,下列说法正确的是( )
| A. | 简单离子半径:X<Y<W | |
| B. | Y、Z两种元素的氧化物均具有两性 | |
| C. | Z、W形成化合物的电子式为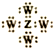 | |
| D. | X、W分别形成的氢化物中所含化学键种类相同 |
1.雾霾严重影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后得试样溶液,设计并完成了如下的实验:
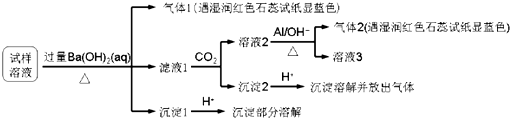
已知:3NO3-+8Al+5OH-+2H2O═3NH3+8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是( )

已知:3NO3-+8Al+5OH-+2H2O═3NH3+8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
| A. | 试样中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| C. | 试样中可能存在Na+、Cl- | |
| D. | 试样中一定不含Al3+ |
15.下列有关物质用途的说法,不正确的是( )
| A. | 高纯度的硅单质广泛用于制造制作光导纤维 | |
| B. | 次氯酸钠具有强氧化性,可用于配制“84”消毒液 | |
| C. | 小苏打可用于治疗胃酸过多 | |
| D. | 过氧化钠可用于潜水艇的氧气来源 |
16.正确认识官能团有助于了解有机物的性质,下列有关物质官能团的说法正确的是( )
| A. | 油脂分子中都含有碳碳双键 | B. | 葡萄糖分子中含有羟基和醛基 | ||
| C. | 水分子中含有羟基 | D. | 乙酸乙酯分子中含有羧基 |
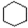 $→_{①}^{Cl_{2}光照}$
$→_{①}^{Cl_{2}光照}$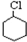 $→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2}不见光}$B$\stackrel{④}{→}$
$→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2}不见光}$B$\stackrel{④}{→}$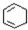 $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$ $\stackrel{⑥}{→}$C$→_{⑦}^{H_{2}}$
$\stackrel{⑥}{→}$C$→_{⑦}^{H_{2}}$
 ,C
,C .
.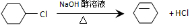 反应⑤
反应⑤ .
.