题目内容
15.下列反应中既属于氧化还原反应又属于放热热反应的是( )| A. | 氢氧化钾与硫酸的反应 | B. | 锌与盐酸反应放出氢气 | ||
| C. | CO2通过炽热的焦炭发生的反应 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
分析 氧化还原反应的特征是元素化合价的升降.反应物总能量大于生成物总能量,则反应为放热反应,反之为吸热反应.
常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),据此分析解答.
解答 解:A.氢氧化钾与硫酸的反应生成硫酸钾和水,为中和反应,没有元素的化合价变化,为非氧化还原反应,且为放热反应,故A不选;
B.锌与盐酸反应生成氯化锌和氢气,Zn、H元素的化合价变化,为氧化还原反应,且为放热反应,故B选;
C.CO2通过炽热的焦炭发生的反应生成一氧化碳,C元素化合价变化,为氧化还原反应,为吸热反应,故C不选;
D.Ba(OH)2•8H2O与NH4Cl反应为非氧化还原反应,也为吸热反应,故D不选;
故选B.
点评 本题考查氧化还原反应和反应中的热效应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应、吸热反应判断的考查,注意归纳常见的放热、吸热反应及从元素化合价角度分析,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
1.下列说法正确的是( )
| A. | 石油液化气的主要成份为甲烷 | |
| B. | 燃料的脱硫、脱氮都是减少酸雨产生的措施 | |
| C. | BaSO4难溶于水是弱电解质,在医学上用作钡餐 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
3.合理利用燃料减小污染符合“绿色化学”理念,下列关于燃料的说法正确的是( )
| A. | “可燃冰”是将水变为油的新型燃料 | |
| B. | 氢气是具有热值高、无污染等优点的燃料 | |
| C. | 天然气、海洋能、太阳能、生物质能、风能、氢能 都属于新能源 | |
| D. | 电能是一次能源 |
10.下列反应中,在原理上可以设计成原电池的是( )
| A. | Ba(OH)2•8H2O与NH4Cl的反应 | B. | NaOH溶液与盐酸的反应 | ||
| C. | 甲烷与氧气的反应 | D. | 石灰石的分解反应 |
20.乙醇中的化学键如图,则下列说法中正确的是( )
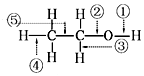

| A. | 当乙醇发生催化氧化时,被破坏的键是②③ | |
| B. | 当乙醇与Na反应时,被破坏的键是① | |
| C. | 当乙醇与乙酸反应时,被破坏的键是② | |
| D. | 当乙醇发生催化氧化时,被破坏的键是①④ |
7.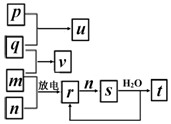 短周期主族元素X、Y、Z、W的原子序数依次增大.在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性.常温下,0.1mol•L-1 t溶液与0.1mol•L-1 u溶液的pH 均为1.下列说法不正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性.常温下,0.1mol•L-1 t溶液与0.1mol•L-1 u溶液的pH 均为1.下列说法不正确的是( )
 短周期主族元素X、Y、Z、W的原子序数依次增大.在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性.常温下,0.1mol•L-1 t溶液与0.1mol•L-1 u溶液的pH 均为1.下列说法不正确的是( )
短周期主族元素X、Y、Z、W的原子序数依次增大.在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性.常温下,0.1mol•L-1 t溶液与0.1mol•L-1 u溶液的pH 均为1.下列说法不正确的是( )| A. | Y、W的最高价氧化物对应的水化物均为强酸 | |
| B. | 元素的非金属性:Z>Y>X,原子半径:X<Z<Y | |
| C. | s溶于水的反应中,氧化剂与还原剂的物质的量之比为1:2 | |
| D. | v的电子式可表示为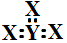 |
4.有X、Y、Z三种原子序数逐渐增大的主族元素,它们分别处于不同短周期,其中Y是自然界中形成化合物种类最多的元素,Z元素在地壳中的含量是同周期主族元素中最高的.则下列说法错误的是( )
| A. | X与其它元素之间只能形成共价键 | |
| B. | Z元素的最高价氧化物是玻璃的主要成分,其常温下就能与强碱发生反应 | |
| C. | 非金属性Y强于Z | |
| D. | 三种元素中X的原子半径最小 |
 .
.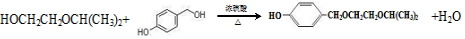 .
.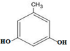 、
、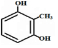 .
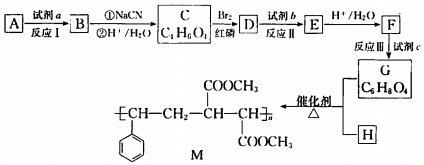
.
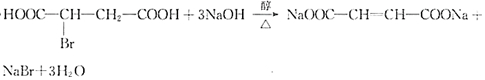 .
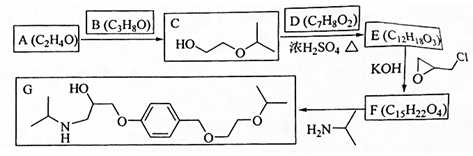
.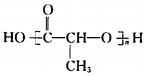 在该条件下,1mol N生成2mol I,N的结构简式是
在该条件下,1mol N生成2mol I,N的结构简式是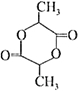 .
.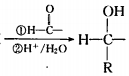 以苯和乙醛为原料制备H,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
以苯和乙醛为原料制备H,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):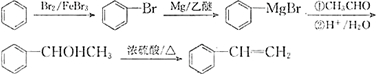 .
.