题目内容
12.下列有关物质性质的应用正确的是( )| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 氯化铝是一种电解质,可用于电解制铝 |
分析 A.液氨汽化时要吸收大量的热;
B.两性氧化物是与酸、碱反应都只生成盐和水;
C.一氧化氮不稳定,容易被氧化生成二氧化氮;
D.氯化铝属于共价化合物,熔融情况下不导电.
解答 解:A.液氨汽化时要吸收大量的热,可用作制冷剂,故A正确;
B.氢氟酸与二氧化硅反应生成四氟化硅和水,不符合两性氧化物的概念,不是两性氧化物,故B错误;
C.一氧化氮不稳定,容易被氧化生成二氧化氮,故C错误;
D.氯化铝属于共价化合物,熔融情况下不导电,不能用于电解制铝,故D错误;
故选:A.
点评 本题考查物质的性质和用途,熟悉氨气、二氧化硅、氯化铝的性质是解题关键,注意两性氧化物的概念,题目难度不大.

练习册系列答案
相关题目
2.下列为无色透明且能在强酸性溶液中大量共存的离子组是( )
| A. | Fe3+、Cu2+、SO42-、Cl- | B. | K+、Na+、HCO3-、NO3- | ||
| C. | Al3+、NH4+、Cl-、NO3- | D. | Ca2+、Ba2+、CO32-、SO42- |
3. 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
 室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1 NaOH溶液分别滴定20.00ml 0.100mol•L-1 的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是( )| A. | II表示的是滴定醋酸的曲线 | |
| B. | V(NaOH)=20.00ml时,两份溶液中c(Cl-)=c(CH3COO-) | |
| C. | pH=7时,滴定醋酸消耗V(NaOH)小于20ml | |
| D. | V(NaOH)=10.00ml时,醋酸溶液中:2c(OH-)-2 c(H+ )=c(CH3COO-)-c(CH3COOH) |
20.将3.9g镁铝合金,投入到500mL 2mol/L的盐酸中,金属完全溶解,再加入4mol/L的NaOH溶液,若要生成的沉淀最多,加入的这种NaOH溶液的体积是( )
| A. | 125 mL | B. | 200 mL | C. | 250 mL | D. | 560 mL |
7.下列实验中,依据实验操作及现象,得出的结论不正确的是( )
| 操 作 | 现 象 | 结 论 | |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| B | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化 但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
| C | 无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中可能含有 CO32-或 HCO3- |
| A. | A | B. | B | C. | C | D. | D |
17.用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 1 mol 过氧化钠与水反应时转移电子数为2NA | |
| B. | 16g氧气中所含的电子数为NA | |
| C. | 22.4L氯化氢溶于水可电离出1mol Cl- | |
| D. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
4.根据有机化合物的命名原则,下列命名正确的是( )
| A. | CH3CH=C(CH3) CH3 3-甲基-2-丁烯 | |
| B. | CH3CH(CH3)CH(Cl)CH3 3-甲基-2-氯丁烷 | |
| C. | CH3CH(OH)CH2CH3 2-羟基丁醇 | |
| D. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 |
1.将一块光洁的铁片放入100mL某浓度的硝酸中,当反应不再有气体放出时,取出铁片洗净晾干称重,发现铁片质量减少了4.2g.则该硝酸的浓为( )
| A. | 1.5mol/L | B. | 3.0mol/L | C. | 2.0mol/L | D. | 无法计算 |
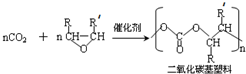 (-R、-R′代表烃基或氢原子)
(-R、-R′代表烃基或氢原子)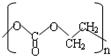 的单体是CO2和
的单体是CO2和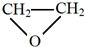 .
.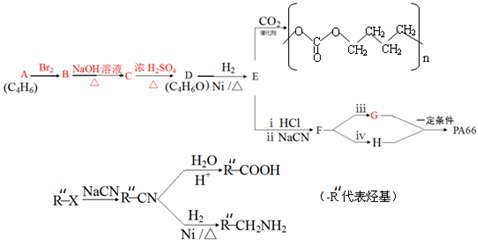
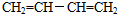 ,名称是1,3-丁二烯.
,名称是1,3-丁二烯.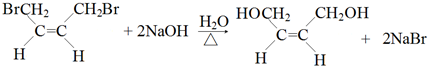 .
.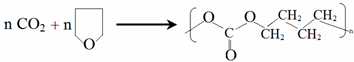 .
.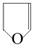 .
. .
. .
.