题目内容
A(g)+3B(g)?2C(g)△H<0达到平衡,改变下列条件,正反应速率始终增大,直达到新平衡的是( )
| A.升温 | B.加压 | C.增大c(A) | D.降低c(C) |
A.该反应是放热反应,升高温度,平衡向逆反应方向移动,所以正反应速率始终增大,直达到新平衡,故A符合;
B.增大压强,平衡向正反应方向移动,则正反应速率先增大后减小,只达到新平衡,故B不符合;
C.增大A的浓度,平衡向正反应方向移动,则正反应速率先增大后减小,只达到新平衡,故C不符合;
D.降低C的浓度,平衡向正反应方向移动,则正反应速率始终减小,只达到新平衡,故D不符合;
故选A.
B.增大压强,平衡向正反应方向移动,则正反应速率先增大后减小,只达到新平衡,故B不符合;
C.增大A的浓度,平衡向正反应方向移动,则正反应速率先增大后减小,只达到新平衡,故C不符合;
D.降低C的浓度,平衡向正反应方向移动,则正反应速率始终减小,只达到新平衡,故D不符合;
故选A.

练习册系列答案
相关题目
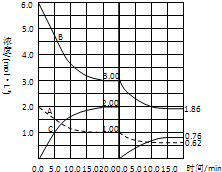 在恒容条件下发生反应A(g)+3B(g)
在恒容条件下发生反应A(g)+3B(g)| 催化剂 |
改变其他反应条件,在Ⅰ、Ⅱ阶段体系中各物质浓度随时间变化的曲线如图所示,下列说法中正确的是( )
| A、第Ⅰ阶段用C表示的平衡前的反应速率v (C)=0.1 mol/(L?S) |
| B、第Ⅱ阶段中B的平衡转化率αⅡ(B)为0.019 |
| C、第Ⅰ阶段的平衡常数KⅠ与第Ⅱ阶段平衡常数KⅡ的大小关系是:KⅠ<KⅡ |
| D、由第一次平衡到第二次平衡,可能采取的措施是从反应体系中移出产物C |
反应A(g)+3B(g)=2C(g)+2D(g)在四种不同的情况下的反应速率分别如下,其中反应速率最大的是( )
| A、v(A)=0.15mol/(L?min) | B、v(B)=0.6mol/(L?min) | C、v(C)=0.4mol/(L?min) | D、v(D)=0.5mol/(L?min) |
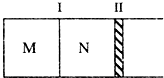 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )| A、起始时,分别向M、N两个容器中加入1molA、1molC,达平衡时,容器M、N中物质A的体积分数相同 | B、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中物质A的转化率较大 | C、起始时,分别向M、N两个容器中加入2molC,容器N达到平衡所需的时间较短 | D、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中气体的密度较大 |
