题目内容
6.同温同压下,同体积的CO和CO2,下列说法不正确的是( )| A. | 分子数之比为1:1 | B. | 密度之比为3:2 | ||
| C. | 质量之比为7:11 | D. | 质子数之比为7:11 |
分析 同温同压下,相同体积的气体含有相同分子数目、相同的物质的量,结合每个分子含有原子数目和质子数目计算原子总数之比,根据m=nM判断质量之比.
解答 解:A.依据阿伏伽德罗定律可知,同温同压下,相同体积的气体含有相同分子数目,故A正确;
B.同温同压下,气体密度之比等于摩尔质量之比,则同温同压下,同体积的CO和CO2,密度之比为28:44=7:11,故B错误;
C.同温同压下,同体积的CO和CO2的物质的量相等,根据m=nM,可知二者质量之比=28g/mol:44g/mol=7:11,故C正确;
D.同温同压下,同体积的CO和CO2含有相同分子数目,则含有质子数之比等于(6+8):(6+16)=14:22=7:11,故D正确;
故选:B.
点评 本题考查阿伏伽德罗定律、微粒数目计算,比较基础,注意根据PV=nRT理解阿伏伽德罗定律及其推论,题目难度不大.

练习册系列答案
相关题目
19.对溶液中的离子进行鉴定,下列实验所得结论不合理的是( )
| A. | 某未知气体通入品红溶液中,品红溶液褪色,则原气体不一定是SO2 | |
| B. | 向溶液中加入KSCN溶液,观察无明显现象,继续加入氯水,溶液变红色,说明溶液中一定含有Fe2+ | |
| C. | 向溶液中加入NaOH溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推测该溶液中含有NH4+ | |
| D. | 向溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体,可推测溶液中一定含有CO32- |
17.两种短周期元素X、Y能形成化合物XY2,已知其原子序数分别为a和b,则a不可能是( )
| A. | b+4 | B. | b-1 | C. | b+6 | D. | b+8 |
14.我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其它材料电池,电池总反应为:V2O5+xLi $?_{充电}^{放电}$LixV2O5.下列说法中,正确的是( )
| A. | 锂在放电时做正极材料,充电时为阳极材料 | |
| B. | 电池在放电时,Li+向负极移动 | |
| C. | 该电池充电时阳极的反应为:LixV2O5-xe-=V2O5+xLi+ | |
| D. | V2O5只是锂发生反应的载体,不参与电池反应 |
1.有下列仪器:①集气瓶 ②量筒 ③烧杯 ④表面皿 ⑤蒸发皿 ⑥容量瓶 ⑦圆底烧瓶 能够用于加热的( )
| A. | ②③⑤ | B. | ③⑥⑦ | C. | ①③④ | D. | ③⑤⑦ |
11.下列结论中错误的是( )
①微粒半径:K+>Al3+>Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:F->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:K+>Al3+>Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:F->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | ① | B. | ①③ | C. | ②④⑤⑥⑦ | D. | ①③⑤ |
18.在无色溶液中能大量共存的一组离子是( )
| A. | Fe3+、SCN-、CO32-、K+ | B. | SO32-、S2-、Al3+、Na+ | ||
| C. | NO3-、CH3COO-、Ba2+、Cl- | D. | SO42-、NH4+、ClO-、I- |
15.如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
已知:2KMnO4+16HCl(浓)═2KCl+5Cl2↑+2MnCl2+8H2O
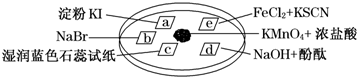
对实验现象的“解释或结论”正确的是( )
已知:2KMnO4+16HCl(浓)═2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝 | 氧化性:Cl2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变血红色 | 还原性:Fe2+>Cl- |
| A. | A | B. | B | C. | C | D. | D |
15.13153I是常规核裂变的产物之一,可以通过测定大气或者水中的13153I 的含量来监测核电站是否发生发射性物质泄漏.下列有关 的叙述中错误的是( )
| A. | 13153I 的化学性质与12753I 相同 | |
| B. | 13153I 的原子序数为53 | |
| C. | 13153I 的原子核外电子数为78 | |
| D. | 13153I 的原子核内中子数多于质子数 |