题目内容
下列说法正确的是( )
| A、难溶电解质作比较时,Ksp小的,溶解度一定小 |
| B、Ksp大小取决于难溶电解质的量,所以离子浓度改变时,沉淀平衡会发生移动 |
| C、所谓沉淀完全就是用沉淀剂将溶液中某一离子完全除去 |
| D、温度一定,当溶液中Ag+ 和Cl-浓度的乘积等于Ksp时,溶液为AgCl的饱和溶液 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:A、溶度积常数与溶解度的大小比较不一定完全一致,要分子二者的结构是否相似;
B、Ksp的大小与温度有关,与难溶电解质的量无关;
C、难溶电解质在溶液中存在溶解平衡;
D、溶液中的离子浓度幂之积等于溶度积常数时,为饱和溶液.
B、Ksp的大小与温度有关,与难溶电解质的量无关;
C、难溶电解质在溶液中存在溶解平衡;
D、溶液中的离子浓度幂之积等于溶度积常数时,为饱和溶液.
解答:
解:A、只有具有相同结构的难溶物(如AgCl、AgBr、AgI)Ksp小的溶解度小,而不同结构的(如Ag2SO4和AgI)Ksp小的溶解度不一定小,故A错误;
B、Ksp的大小与温度有关,与难溶电解质的量无关,而平衡移动与离子浓度有关,故B错误;
C、难溶电解质在溶液中存在溶解平衡,不可能加入沉淀剂将溶液中某一离子除净,故C错误;
D、当溶液中的离子浓度幂之积等于溶度积常数时,为饱和溶液,故D正确.
故选D.
B、Ksp的大小与温度有关,与难溶电解质的量无关,而平衡移动与离子浓度有关,故B错误;
C、难溶电解质在溶液中存在溶解平衡,不可能加入沉淀剂将溶液中某一离子除净,故C错误;
D、当溶液中的离子浓度幂之积等于溶度积常数时,为饱和溶液,故D正确.
故选D.
点评:本题考查难溶电解质的溶解平衡及沉淀转化的本质,本题难度不大,侧重于对概念的理解.

练习册系列答案
相关题目
SiO2是水晶的主要成分,SiO2属于( )
| A、酸 | B、碱 | C、盐 | D、氧化物 |
下列物质的水溶液呈碱性的是( )
| A、K2SO4 |
| B、NH4Cl |
| C、Na2CO3 |
| D、H2SO3 |
在做中和热实验测定中和热时,应使用的仪器正确的组合是:( )
①量筒 ②托盘天平 ③烧杯 ④容量瓶 ⑤冷凝管 ⑥温度计 ⑦酒精灯.
①量筒 ②托盘天平 ③烧杯 ④容量瓶 ⑤冷凝管 ⑥温度计 ⑦酒精灯.
| A、①③⑥ | B、②③⑤ |
| C、①②③⑥ | D、全部 |
化学反应N2+3H2→2NH3的能量变化如图所示,该反应的热化学方程式是( )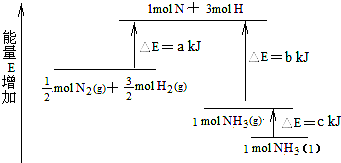
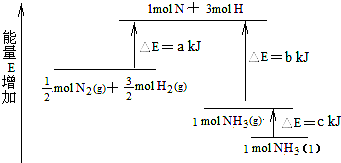
A、
| ||||
B、
| ||||
| C、N2(g)+3 H2(g)→2 NH3(g);△H=2(b-a)kJ/mol | ||||
| D、N2(g)+3 H2(g)→2 NH3(1);)△H=2(a-b-c)kJ/mol |
在工业生产中,降低能耗是重要的节能措施.下列说法不符合生产实际的是( )
| A、使用恰当的还原剂,可以在较低的温度下把金属从矿石中提取出来 |
| B、研制出性能优良的催化剂可以使反应温度降低,提高反应速率,从而起到节能效果 |
| C、制水泥、玻璃等硅酸盐工业需要消耗大量能源,我们应通过降低其产量来节能 |
| D、利用铝的还原性和铝转化为氧化铝时能放出大量热的性质,工业上常用铝粉来还原一些金属氧化物 |
下列说法中正确的是(NA表示阿伏伽德罗常数)( )
| A、28g N2所含有的原子数为NA |
| B、1.8g的NH4+离子中含有电子数11NA |
| C、22.4LCH4的质量与NA个甲烷分子的质量之和相等 |
| D、标准状况下,22.4LCH4和O2的混合气体所含有的分子数为NA |