题目内容
10.设NA为阿伏加德罗常数的值.下列叙述正确的是(C-12 N-14 O-16)( )| A. | 标准状况下,11.2 L甲烷中含有的碳氢键数目为2NA | |
| B. | 常温下,1L 0.1mol/L的Na2CO3溶液中含有OH-离子数为0.1NA | |
| C. | 常温常压下,28 g N2、CO的混合气体中含有N2分子数为0.5NA | |
| D. | 标准状况下,22.4 L Cl2与足量NaOH溶液反应,转移的电子数为2NA |
分析 A、求出甲烷的物质的量,然后根据1mol甲烷中含4mol碳氢键来分析;
B、常温下,1L 0.1mol/L的Na2CO3溶液由于水解显碱性,但碱性较弱;
C、混合气体中氮气和CO的比例不确定;
D、求出氯气的物质的量,然后根据氯气和碱的反应为歧化反应来分析.
解答 解:A、标况下11.2L甲烷的物质的量为0.5mol,而1mol甲烷中含4mol碳氢键,故0.5mol甲烷中含碳氢键为2NA个,故A正确;
B、常温下,1L 0.1mol/L的Na2CO3溶液由于水解显碱性,但水解程度很小故碱性较弱,即溶液中的氢氧根的浓度小于0.1mol/L,则在1L溶液中,氢氧根的个数小于0.1NA个,故B错误;
C、混合气体中氮气和CO的比例不确定,故28g即1mol两者的混合物中,氮气分子个数无法确定,故C错误;
D、标况下22.4L氯气的物质的量为1mol,而氯气和碱的反应为歧化反应,故1mol氯气和碱反应转移NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
20.下列有关溶液中离子存在和转化的表达合理的是( )
| A. | 中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- | |
| B. | 标准状况下,将1.12 L CO2气体通入1 L 0.1 mol/L的NaAlO2溶液中:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 由水电离出的c(H+)=1×10-12 mol/L 的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| D. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═NH3•H2O+Al(OH)3↓+2BaSO4↓ |
18.设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A. | 1 mol Cl2与足量Ca(OH)2溶液反应,转移的电子数为NA | |
| B. | 1 mol碳烯(:CH2)所含的电子数目为6 NA | |
| C. | 常温常压下,11.2 L甲烷中含有的氢原子数小于2 NA | |
| D. | 某温度时,1 L pH=6的纯水中含OH-数为10-6NA |
5.下列电解质溶液有关叙述正确的是( )
| A. | 恒温条件下稀释氢氟酸时,HF的Ka增大,水的KW不变 | |
| B. | 向Mg(OH)2沉淀悬浊液中加入NH4Cl固体,c(Mg2+)、c(OH-)浓度均增大 | |
| C. | 0.1mol/LNaHCO3溶液中,c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 0.1mol/LNa2SO3溶液中,加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
2.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 0.1mol•L-1的NH4NO3溶液中含有的氮原子数为0.2NA | |
| B. | 1 mol氯气分别与足量铁和铝完全反应时转移的电子数均为3NA | |
| C. | 16g O2和16g O3均含有NA个氧原子 | |
| D. | 25℃时1L pH=1的H2SO4溶液中含有H+的数目为0.2NA |
19.下列说法正确的是( )
| A. | 已知C-C键可以绕键轴自由旋转,结构简式为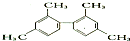 的分子中至少有11个碳原子处于同一平面上 的分子中至少有11个碳原子处于同一平面上 | |
| B. | 苯中含有杂质苯酚,可用浓溴水来除杂 | |
| C. | 1mo1 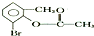 在一定条件下与足量NaOH溶液反应,最多消耗3 mol NaOH 在一定条件下与足量NaOH溶液反应,最多消耗3 mol NaOH | |
| D. | 按系统命名法,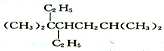 的名称为3,3,6一三甲基-4-乙基庚烷 的名称为3,3,6一三甲基-4-乙基庚烷 |
 .
. 在一个U形管里盛有氯化铜溶液,并插入Zn片和C棒作电极,按下图连接.
在一个U形管里盛有氯化铜溶液,并插入Zn片和C棒作电极,按下图连接.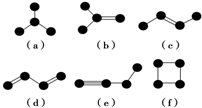 如图是由4个碳原子结合成的6种有机物(氢原子没有画出).
如图是由4个碳原子结合成的6种有机物(氢原子没有画出).