题目内容
碳及其化合物在生活中应用广泛.①将小块金刚石镶在玻璃刀头上用来裁玻璃; ②将石墨用于制作电极;
③一氧化碳用作气体燃料; ④干冰用于人工降雨;
⑤一氧化碳可用于炼铁.
(1)上述用途中,主要利用了物质的物理性质的有 .(填序号)
(2)除④以外,写出二氧化碳的一条用途 .
(3)干冰的物质类型不属于 .(填序号)
A.混合物 B.纯净物 C.化合物 D.氧化物
(4)一氧化碳与赤铁矿(主要成分Fe2O3)炼铁反应的化学方程式为 .
(5)一氧化碳燃烧时火焰呈蓝色,该反应的化学方程式为 .
(6)在汽车尾气系统中装置催化转化器,可将一氧化碳和一氧化氮有毒气体转化为无毒的二氧化碳和氮气,该反应的化学方程式为 .
【答案】分析:(1)物理性质包含:色、态、味、熔沸点、密度、硬度、导电性等;
(2)二氧化碳不支持燃烧,能灭火;
(3)A.含有两种或两种以上的物质是混合物;
B.只含一种物质的是纯净物;
C.含有两种或两种以上元素的纯净物是化合物;
D.有两种元素组成其中一种元素是氧元素的纯净物是氧化物;
(4)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
(5)一氧化碳燃烧生成二氧化碳;
(6)在催化剂条件下,一氧化碳和一氧化氮反应生成氮气和二氧化碳.
解答:解:(1)物理性质包含:色、态、味、熔沸点、密度、硬度、导电性等,所以上述用途中,①将小块金刚石镶在玻璃刀头上用来裁玻璃是利用了金刚石的高硬度; ②将石墨用于制作电极是利用了石墨的导电性;
④干冰用于人工降雨是利用了干冰升华时能吸收热量;主要利用了物质的物理性质的有①②④,故答案为:①②④;
(2)二氧化碳不支持燃烧,所以能灭火,故答案为:灭火;
(3)干冰是固体二氧化碳,干冰中只含一种物质是纯净物;有两种元素组成,所以化合物;有两种元素组成,其中一种是氧元素,所以是氧化物,故选A;
(4)高温条件下,氧化铁被一氧化碳还原生成铁,同时自身被氧化生成二氧化碳,反应方程式为3CO+Fe2O3 2Fe+3CO2,
2Fe+3CO2,
故答案为:3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
(5)点燃条件下,一氧化碳燃烧生成二氧化碳,反应方程式为:2CO+O2 2CO2,故答案为:2CO+O2
2CO2,故答案为:2CO+O2 2CO2;
2CO2;
(6)在催化剂条件下,一氧化碳和一氧化氮反应生成氮气和二氧化碳,反应方程式为2NO+2CO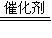 N2+2CO2,故答案为:2NO+2CO
N2+2CO2,故答案为:2NO+2CO N2+2CO2.
N2+2CO2.
点评:本题考查了物质的性质和用途,性质决定用途,用途体现性质,难度不大,注意基础知识的积累.
(2)二氧化碳不支持燃烧,能灭火;
(3)A.含有两种或两种以上的物质是混合物;
B.只含一种物质的是纯净物;
C.含有两种或两种以上元素的纯净物是化合物;
D.有两种元素组成其中一种元素是氧元素的纯净物是氧化物;
(4)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
(5)一氧化碳燃烧生成二氧化碳;
(6)在催化剂条件下,一氧化碳和一氧化氮反应生成氮气和二氧化碳.
解答:解:(1)物理性质包含:色、态、味、熔沸点、密度、硬度、导电性等,所以上述用途中,①将小块金刚石镶在玻璃刀头上用来裁玻璃是利用了金刚石的高硬度; ②将石墨用于制作电极是利用了石墨的导电性;
④干冰用于人工降雨是利用了干冰升华时能吸收热量;主要利用了物质的物理性质的有①②④,故答案为:①②④;
(2)二氧化碳不支持燃烧,所以能灭火,故答案为:灭火;
(3)干冰是固体二氧化碳,干冰中只含一种物质是纯净物;有两种元素组成,所以化合物;有两种元素组成,其中一种是氧元素,所以是氧化物,故选A;
(4)高温条件下,氧化铁被一氧化碳还原生成铁,同时自身被氧化生成二氧化碳,反应方程式为3CO+Fe2O3
 2Fe+3CO2,
2Fe+3CO2,故答案为:3CO+Fe2O3
 2Fe+3CO2;
2Fe+3CO2;(5)点燃条件下,一氧化碳燃烧生成二氧化碳,反应方程式为:2CO+O2
 2CO2,故答案为:2CO+O2
2CO2,故答案为:2CO+O2 2CO2;
2CO2;(6)在催化剂条件下,一氧化碳和一氧化氮反应生成氮气和二氧化碳,反应方程式为2NO+2CO
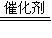 N2+2CO2,故答案为:2NO+2CO
N2+2CO2,故答案为:2NO+2CO N2+2CO2.
N2+2CO2.点评:本题考查了物质的性质和用途,性质决定用途,用途体现性质,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
 (2010?天河区二模)铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
(2010?天河区二模)铁及其化合物在日常生活应用广泛,请根据下列实验回答问题:
 HCO3-+OH-
HCO3-+OH-
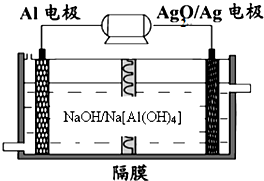 (2013?青岛一模)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
(2013?青岛一模)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.