题目内容
4.常温下,下列溶液的pH大于7的是( )| A. | NH4Cl | B. | Al2(SO4)3 | C. | NaHCO3 | D. | Na2SO4 |
分析 常温下,下列溶液的pH大于7的溶液显碱性,是碱溶液或强碱弱酸盐溶液,据此分析.
解答 解:A、氯化铵是强酸弱碱盐,其溶液水解显酸性,pH小于7,故A错误;
B、硫酸铝是强酸弱碱盐,其水溶液水解显酸性,pH小于7,故B错误;
C、碳酸氢钠是强碱弱酸盐,碳酸氢根在溶液中既能水解又能电离,且水解大于电离,故溶液显碱性,即pH大于7,故C正确;
D、硫酸钠是强酸强碱的正盐,在溶液中不能电离出氢离子或氢氧根,也不能水解,故溶液显中性,故D错误.
故选C.
点评 本题考查了溶液的酸碱性,应注意的是显酸性的溶液不一定是酸溶液,显碱性的溶液不一定是碱溶液.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
14.下列有关化学用语表示正确的是( )
| A. | HClO的结构式:H-Cl-O | B. | 氨气分子的比例模型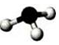 | ||
| C. | 原子核内有10个中子的氧原子:18O | D. | H2与H+互为同位素 |
15.下列元素中,原子半径最大的是( )
| A. | Na | B. | Al | C. | P | D. | S |
9.离子方程式CO32-+2H+=CO2+H2O可表示的反应是( )
| A. | 可溶性碳酸盐与强酸反应生成CO2和H2O | |
| B. | 难溶的碳酸盐和难电离的酸反应生成CO2和H2O | |
| C. | 可溶性碳酸盐与任何酸溶液反应生成CO2和H2O | |
| D. | 石灰石和盐酸反应制取CO2 |
16.下列离子方程式中,书写正确的是( )
| A. | 氢氧化镁溶于盐酸:OH-+H+═H2O | |
| B. | 铜片插入硝酸银溶液中:Cu+Ag+═Ag++Cu2+ | |
| C. | 将稀硫酸加入氢氧化钡溶液:H++OH-═H2O | |
| D. | 碳酸钠溶液与稀硫酸混合:CO32-+2H+═CO2↑+H2O |
13.NA表示阿伏伽德罗常数,则下列说法正确的是( )
| A. | 1 L 0.1 mol/LNaHSO4溶液中含有0.1 NA个HSO4- | |
| B. | 已知反应:5Cl-+ClO3-+6H+=3Cl2+3H2O,每生成71g Cl2,则转移2NA个电子 | |
| C. | 乙烯(C2H4)和环丙烷(C3H6)组成的28g混合气体中含有氢原子数为4NA个 | |
| D. | 标准状况下,22.4LCCl4中含有NA个CCl4分子 |
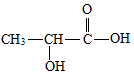 乳酸是世界上公认的三大有机酸之一,其应用非常广泛,可用作食品酸味剂、医药防腐剂、工业pH调节剂等.乳酸的结构简式如图所示.
乳酸是世界上公认的三大有机酸之一,其应用非常广泛,可用作食品酸味剂、医药防腐剂、工业pH调节剂等.乳酸的结构简式如图所示.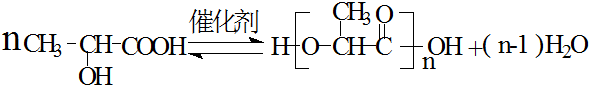 .
.