题目内容
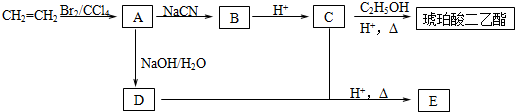
16.【有机化学基础】工业上常以烃的含氧衍生物X为主要原料生产可降解塑料PCL【H[O(CH2)5CO]nOH]】及阻燃剂四溴双酚A. 合成线路如下:
已知:①X的蒸汽密度是相同条件下H2的47倍,遇FeCl3溶液显紫色;

(1)B的分子式为C6H12O;C中官能团的电子式为
 ;D的结构简式为
;D的结构简式为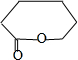 .
.(2)B→C还需要的反应试剂及条件是O2、Cu、加热,该反应类型是氧化反应.
(3)写出E→PCL的化学方程式:nHO(CH2)5COOH$→_{△}^{催化剂}$
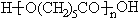 +(n-1)H2O;
+(n-1)H2O;写出X→Y的化学方程式:
 ;
;(4)符合以下条件的D的同分异构体有10种(不考虑空间异构),任意写出其中一种的结构简式为HCOOCH=CHCH(CH3)2.
①能使溴的CCl4溶液褪色 ②能发生银镜反应 ③含有两个甲基和两种官能团
(5)已知由烯烃直接制备不饱和酯的新方法为:

利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料,
 写出合成该涂料的反应流程图
写出合成该涂料的反应流程图 .
.
分析 X的蒸汽密度是相同条件下H2的47倍,其相对分子质量为47×2=94,遇FeCl3溶液显紫色,说明含有酚羟基,则X为 ,X和氢气发生加成反应生成B为
,X和氢气发生加成反应生成B为 ,C为
,C为 ,则B发生催化氧化反应生成C,PCL为E发生缩聚反应产物,则E结构简式为HO(CH2)5COOH,D发生水解反应然后酸化得到E,结合信息可知D的结构简式为
,则B发生催化氧化反应生成C,PCL为E发生缩聚反应产物,则E结构简式为HO(CH2)5COOH,D发生水解反应然后酸化得到E,结合信息可知D的结构简式为 .根据题给信息②知,Y结构简式为
.根据题给信息②知,Y结构简式为 ,四溴双酚A结构简式为
,四溴双酚A结构简式为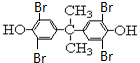 .
.
(5)一定条件下乙烯和水发生加成反应生成CH3CH2OH,CH3CH2OH和CH2=CH2、CO、O2反应生成CH2=CHCOOCH2CH3,CH2=CHCOOCH2CH3发生加聚反应生成高分子化合物.
解答 解:X的蒸汽密度是相同条件下H2的47倍,其相对分子质量为47×2=94,遇FeCl3溶液显紫色,说明含有酚羟基,则X为 ,X和氢气发生加成反应生成B为
,X和氢气发生加成反应生成B为 ,C为
,C为 ,则B发生催化氧化反应生成C,PCL为E发生缩聚反应产物,则E结构简式为HO(CH2)5COOH,D发生水解反应然后酸化得到E,结合信息可知D的结构简式为
,则B发生催化氧化反应生成C,PCL为E发生缩聚反应产物,则E结构简式为HO(CH2)5COOH,D发生水解反应然后酸化得到E,结合信息可知D的结构简式为 .根据题给信息②知,Y结构简式为
.根据题给信息②知,Y结构简式为 ,四溴双酚A结构简式为
,四溴双酚A结构简式为 .
.
(1)B为环己醇,其分子式为C6H12O,C为 ,官能团的电子式为
,官能团的电子式为 ,D的结构简式为
,D的结构简式为 ,
,
故答案为:C6H12O; ;
; ;
;
(2)B→C还需要的反应试剂及条件是O2、Cu、加热,C生成D的反应是氧化反应,
故答案为:O2、Cu、加热;氧化反应;
(3)E→PCL的化学方程式:nHO(CH2)5COOH$→_{△}^{催化剂}$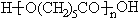 +(n-1)H2O,
+(n-1)H2O,
X→Y的化学方程式: ,
,
故答案为:nHO(CH2)5COOH$→_{△}^{催化剂}$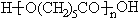 +(n-1)H2O;
+(n-1)H2O; ;
;
(4)D结构简式为 ,D的同分异构体符合下列条件:①能使溴的CCl4溶液褪色,②能发生银镜反应,③含有两个甲基和两种官能团,说明含有碳碳双键与醛基,符合条件的同分异构体有:HCOOCH2CH=C(CH3)2、HCOOC(CH3)CH=CH2、HCOOCH(CH3)CH=CHCH3、HCOOCH(CH3)C(CH3)=CH2、HCOOCH2C(CH3)=CH2CH3、HCOOC(CH2CH3)=CHCH3、HCOOC(CH3)=C(CH3)CH3、HCOOC(CH3)=CHCH2CH3、HCOOCH=C(CH3)CH3、HCOOCH=CHCH(CH3)2,共10种,
,D的同分异构体符合下列条件:①能使溴的CCl4溶液褪色,②能发生银镜反应,③含有两个甲基和两种官能团,说明含有碳碳双键与醛基,符合条件的同分异构体有:HCOOCH2CH=C(CH3)2、HCOOC(CH3)CH=CH2、HCOOCH(CH3)CH=CHCH3、HCOOCH(CH3)C(CH3)=CH2、HCOOCH2C(CH3)=CH2CH3、HCOOC(CH2CH3)=CHCH3、HCOOC(CH3)=C(CH3)CH3、HCOOC(CH3)=CHCH2CH3、HCOOCH=C(CH3)CH3、HCOOCH=CHCH(CH3)2,共10种,
故答案为:10;HCOOCH=CHCH(CH3)2等;
(5)一定条件下乙烯和水发生加成反应生成CH3CH2OH,CH3CH2OH和CH2=CH2、CO、O2反应生成CH2=CHCOOCH2CH3,CH2=CHCOOCH2CH3发生加聚反应生成高分子化合物,合成路线流程图为: ,
,
故答案为: .
.
点评 本题考查有机推断和有机合成,侧重考查学生分析推理及知识综合应用能力,注意对题目给予信息的理解,熟练掌握官能团的性质与衍变,(4)中限制条件同分异构体的书写为易错点、难点,题目难度中等.

| A. | 工业上漂白粉是由氯气和石灰乳制成的 | |
| B. | 漂白粉的主要成分是氯化钙和次氯酸钙 | |
| C. | 漂白粉漂白有色布条时,次氯酸钙直接起漂白作用 | |
| D. | 用漂白粉溶液漂白有色布条时,加些稀盐酸,漂白速率会加快 |
| A. | 绿色化学的核心是从源头上减少和消除化工生产对环境的污染 | |
| B. | 减少化石燃料使用,有利于降低空气中PM2.5的值 | |
| C. | 淀粉、豆油、蛋白质都是天然高分子化合物 | |
| D. | “地沟油”禁止食用,但可以用来制肥皂 |
| A. | 电池放电时,负极周围溶液的pH不断增大 | |
| B. | 电池放电时总反应是Cd+2NiO(OH)+2H2O═Cd(OH)2+2Ni(OH)2 | |
| C. | 电池充电时,镉(Cd)元素被氧化 | |
| D. | 电池充电时,电池的正极和电源的正极相连接 |
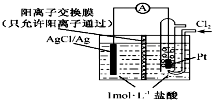 某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )
某原电池装置如右图所示,电池总反应为2Ag+Cl2═2AgCl.已知:阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒.下列说法正确的是( )| A. | 正极反应为AgCl+e-=Ag+Cl- | |
| B. | 电池工作时,交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 若用KCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.2 mol e-时,交换膜左侧溶液中约减少0.4 mol离子 |
| A. | Na最外层有一个电子,Mg最外层有2个电子 | |
| B. | Na能与冷水反应,而Mg不能 | |
| C. | 碱性NaOH>Mg(OH)2 | |
| D. | Na不能从MgCl2的溶液中把Mg置换出来 |
| A. | 硫酸铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 澄清石灰水中加少量碳酸氢钠:Ca2++OH-+HCO${\;}_{3}^{-}$═CaCO3↓+H2O | |
| C. | H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH-+18O2↑ | |
| D. | 碳酸钠的水解反应:CO${\;}_{3}^{2-}$+H3O+?HCO${\;}_{3}^{-}$+H2O |
 +2nH2O.
+2nH2O.