题目内容
 如图是电解饱和食盐水的装置,a、b为石墨电极.下列判断正确的是( )
如图是电解饱和食盐水的装置,a、b为石墨电极.下列判断正确的是( )| A、a为正极,b为负极 |
| B、a极上有氢气放出 |
| C、b极上发生氧化反应 |
| D、b极附近溶液显碱性 |
考点:电解原理
专题:电化学专题
分析:用石墨作电极电解饱和食盐水,
A.连接电源负极的电极为阴极、连接电源正极的电极为阳极;
B.阴极上氢离子放电、阳极上氯离子放电;
C.阳极上发生氧化反应、阴极上发生还原反应;
D.阴极上氢离子放电,同时阴极附近有氢氧根离子生成.
A.连接电源负极的电极为阴极、连接电源正极的电极为阳极;
B.阴极上氢离子放电、阳极上氯离子放电;
C.阳极上发生氧化反应、阴极上发生还原反应;
D.阴极上氢离子放电,同时阴极附近有氢氧根离子生成.
解答:
解:A.根据图象知,a作阳极、b作阴极,故A错误;
B.a电极上氯离子放电生成氯气,所以有氯气生成,故B错误;
C.b电极上氢离子得电子发生还原反应而生成氢气,故C错误;
D.b电极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,导致溶液呈碱性,故D正确;
故选D.
B.a电极上氯离子放电生成氯气,所以有氯气生成,故B错误;
C.b电极上氢离子得电子发生还原反应而生成氢气,故C错误;
D.b电极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,导致溶液呈碱性,故D正确;
故选D.
点评:本题以电解氯化钠溶液为载体考查了电解池原理,明确离子放电顺序是解本题关键,根据阴阳极上得失电子来分析解答,题目难度不大.

练习册系列答案
相关题目
下列各组离子,能在溶液中大量共存的是( )
| A、H+、OH- |
| B、Ba2+、SO42- |
| C、Al3+、OH- |
| D、K+、NO3 |
分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法.下列关于“Na2SiO3”的分类不正确的是( )
| A、离子化合物 | B、电解质 |
| C、钠盐 | D、碱性氧化物 |
下列叙述错误的是( )
| A、Al2(SO4)3可除去酸性废水中的悬浮颗粒 |
| B、氯气与石灰乳反应能得到含氯漂白剂 |
| C、燃煤时加入适量石灰石,可减少废气中SO2的排放 |
| D、工业上硝酸可用于制化肥、农药、炸药和染料等 |
能用离子方程式“H++OH-═H2O”表示的化学反应是( )
A、4HNO3
| ||||
| B、NaOH+HCl=NaCl+H2O | ||||
| C、Fe2O3+6HCl=2FeCl3+3H2O | ||||
D、2H2+O2
|
下列离子方程式书写正确的是( )
| A、Ba(OH)2溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| B、FeCl2溶液与Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
| C、Cu与AgNO3溶液反应:Cu+Ag+=Cu2++Ag |
| D、CaCO3与醋酸反应:CaCO3+2CHCOOH=Ca2++2CHCOO-+CO2↑+H2O |
将盐酸逐滴加入到氨水中,发生反应的离子方程式正确的是( )
| A、OH-+H+=H2O |
| B、H++NH3?H2O=NH4++H2O |
| C、HCl+OH-=Cl-+H2O |
| D、HCl+NH3?H2O=Cl-+NH4++H2O |

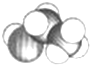 乙醇是生活中常见的一种有机物,它的分子结构模型如图所示:
乙醇是生活中常见的一种有机物,它的分子结构模型如图所示: