题目内容
15.以下是一些原子的2p能级和3d能级中电子排布的情况.其中违反了洪特规则的是( )①

②
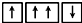
③
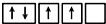
④
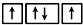
⑤
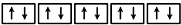
⑥

| A. | ④⑥ | B. | ②③ | C. | ②④⑤ | D. | ②③④⑥ |
分析 洪特规则是指在同一个电子亚层中排布的电子,总是尽先占据不同的轨道,且自旋方向相同,以此进行判断.
解答 解:①2p能层有4个电子,应在3个不同的轨道,符合洪特规则、泡利不相容原理;
②同一轨道自旋方向相同,违反泡利不相容原理,第三个能级中的电子自旋方向和前面的能级相反,违反了洪特规则;
③同一个电子亚层中排布的电子,总是尽先占据不同的轨道,违反了洪特规则;
④2p能级上的4个电子排布符合洪特规则、泡利原理;
⑤3d能级上的10个电子排布符合符合洪特规则、泡利原理;
⑥3d能级上的6个电子排布符合符合洪特规则、泡利原理;
故选B.
点评 本题考查原子核外电子排布规则,难度不大,明确洪特规则的内涵是解题的关键,侧重于洪特规则的应用能力的考查.

练习册系列答案
相关题目
5.铁盐是中学化学常见的盐.下面是以富含硫酸亚铁的工业废液为原料生产氧化铁和制备草酸亚铁晶体(FeC2O3•xH2O )的工艺流程图(部分操作和条件略).

请回答下列问题:
已知:①pH>4时,Fe2+易被氧气氧化;②NH4HCO3在热水中会分解;
③几种物质的溶解度(g/l00g H2O)如下
(1)流程图步骤Ⅰ中,在提纯时需要加足量的铁屑的原因是除去废液中的2Fe3+(或Fe+2Fe3+=3Fe2+).
(2)在生产氧化铁的步骤Ⅲ中,生成FeCO3的离子方程式是Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
(3)上述流程图制备草酸亚铁过程中,用稀硫酸调溶液pH至1〜2的目的是防止亚铁离子水解,防止亚铁离子氧化趁热过滤的原因是增大杂质的溶解度(防止低温时杂质析出),影响产品的纯度.
(4)己知煅烧FeCO3的化学方程式是4FeCO3+O2═2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品.若产品中杂质只有FeO.则该产品中Fe2O3的质量是288.0kg.
(5)已知:某温度时,Ksp(FeC2O4)=1.0×10-6.Ksp(CaC2O4)=2.0×10-9,此温度下,FeC2O4若要在CaCl2溶液中开始转化为CaC2O4,则CaCl2的浓度必须不低于2.0×10-6mol•L-1.
(6)草酸(HzC2O4)是一种二元弱酸,广泛分布于动植物体中.已知0.1mol•L-1KHC2O4溶液呈酸性.下列说法正确的是ac(填字母序号)a、0.1mol•L-1KHC2O4溶液中:c(K+)+c(H+)═c(HC2O4-)+2c(C2O42-)+c(OH- )
b.0.1mol•L-1KHC2O4溶液中:c(K+)>c(HC2O4-)>c((H2C2O4)>c(C2O42-)
C.0.1mol/LKHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+)>c(Na+)
d.浓度均为0.lmol•L-1KHC2O4和K2C2O4的混合溶液中:2c(K+)═c(HC2O4-)+c(C2O42-)

请回答下列问题:
已知:①pH>4时,Fe2+易被氧气氧化;②NH4HCO3在热水中会分解;
③几种物质的溶解度(g/l00g H2O)如下
| FeS04•7H2O | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O | |
| 20℃ | 48 | 75 | 37 |
| 60℃ | 101 | 88 | 38 |
(2)在生产氧化铁的步骤Ⅲ中,生成FeCO3的离子方程式是Fe2++2HCO3-=FeCO3↓+CO2↑+H2O.
(3)上述流程图制备草酸亚铁过程中,用稀硫酸调溶液pH至1〜2的目的是防止亚铁离子水解,防止亚铁离子氧化趁热过滤的原因是增大杂质的溶解度(防止低温时杂质析出),影响产品的纯度.
(4)己知煅烧FeCO3的化学方程式是4FeCO3+O2═2Fe2O3+4CO2.现煅烧464.0kg的FeCO3,得到316.8kg产品.若产品中杂质只有FeO.则该产品中Fe2O3的质量是288.0kg.
(5)已知:某温度时,Ksp(FeC2O4)=1.0×10-6.Ksp(CaC2O4)=2.0×10-9,此温度下,FeC2O4若要在CaCl2溶液中开始转化为CaC2O4,则CaCl2的浓度必须不低于2.0×10-6mol•L-1.
(6)草酸(HzC2O4)是一种二元弱酸,广泛分布于动植物体中.已知0.1mol•L-1KHC2O4溶液呈酸性.下列说法正确的是ac(填字母序号)a、0.1mol•L-1KHC2O4溶液中:c(K+)+c(H+)═c(HC2O4-)+2c(C2O42-)+c(OH- )
b.0.1mol•L-1KHC2O4溶液中:c(K+)>c(HC2O4-)>c((H2C2O4)>c(C2O42-)
C.0.1mol/LKHC2O4溶液中滴加等浓度NaOH溶液至中性:c(K+)>c(Na+)
d.浓度均为0.lmol•L-1KHC2O4和K2C2O4的混合溶液中:2c(K+)═c(HC2O4-)+c(C2O42-)
6.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,该流体在静态时无磁性吸引力,当外加磁场作用时,才表现出磁性,正因如此,它才在实际中有着广泛的应用,在理论上具有很高的学术价值.制备时将等物质的量FeSO4和Fe2(SO4)3溶液混合,滴入稍过量的氢氧化钠溶液,随后加入油酸钠溶液,即可生成黑色的分散质粒子直径在5.5-36nm的磁流体.下列说法中正确的是( )
| A. | 所得的分散系可用过滤的方法进行提纯 | |
| B. | 所得的分散系中分散质为Fe2O3 | |
| C. | 当一束强光通过该分散系时会出现光亮的通路 | |
| D. | 该分散系不稳定 |
3.下列物质的转化在给定条件下不能实现的是( )
| A. | Ca(ClO)2(aq)$\stackrel{CO_{2}}{→}$HClO(aq)$\stackrel{光照}{→}$HCl(aq) | |
| B. | H2SiO3$\stackrel{△}{→}$SiO2$\stackrel{HCl(aq)}{→}$SiCl4 | |
| C. | Al2O3 $→_{△}^{NaOH(ap)}$ NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| D. | Fe2O3$\stackrel{H_{2}SO_{4}(aq)}{→}$Fe2(SO4)3(aq)$\stackrel{△}{→}$无水Fe2(SO4)3 |
10.下表中对“2”的含义解释正确的一组是( )
| ${\;}_{1}^{2}$H | 2He | 2Cl | Ba2+ | |
| A | 质量数 | 中子数 | 质子数 | 电荷数 |
| B | 质量数 | 质子数 | 原子个数 | 电荷数 |
| C | 质子数 | 中子数 | 原子个数 | 电荷数 |
| D | 质量数 | 质子数 | 中子数 | 电荷数 |
| A. | A | B. | B | C. | C | D. | D |
20.下列物质中互为同系物的是( )
| A. | 甲烷与丙烷 | B. | 乙醇与乙酸 | ||
| C. | 一氯甲烷与二氯甲烷 | D. | 正丁烷与异丁烷 |
5.某课外实验小组设计的下列实验合理的是( )
| A. | 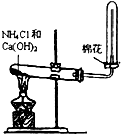 制备少量氨气 | B. | 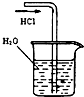 吸收HCl | ||
| C. |  分离苯和乙醇的混合物 | D. | 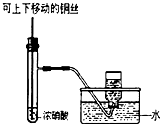 制备并收集少量NO2气体 |
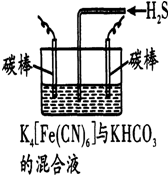 铁和铜是人类使用最早的金属,铁、铜及其化合物在工农业生产等许多领域中有着重要的作用.
铁和铜是人类使用最早的金属,铁、铜及其化合物在工农业生产等许多领域中有着重要的作用.