题目内容
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 0.1 mol•L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA | |
| B. | 标准状况下,11.2 L CCl4中含有的分子数目为0.5NA | |
| C. | 4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2 NA | |
| D. | 1 mol CH5+中含有的电子数目为11NA |
分析 A、溶液体积不明确;
B、标况下四氯化碳为液态;
C、NO2和N2O4的最简式均为NO2;
D、CH5+中含10个电子.
解答 解:A、溶液体积不明确,故溶液中镁离子的个数无法计算,故A错误;
B、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、NO2和N2O4的最简式均为NO2,故4.6g混合物中含有的NO2的物质的量为n=$\frac{4.6g}{46g/mol}$=0.1mol,故含0.2mol氧原子即0.2NA个,故C正确;
D、CH5+中含10个电子,故1molCH5+中含10mol电子即10NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
13.下列说法中正确的是( )
| A. | 物质的量就是物质的质量 | |
| B. | 2mol H2O 可以说为水分子的摩尔数为2mol | |
| C. | 物质的量是以摩尔为单位计量粒子数目的物理量 | |
| D. | 物质的量和摩尔都是含有一定数目粒子的集体 |
10.下列反应中,属于取代反应的是( )
| A. | CH3CH=CH2+Br2$\stackrel{CCl_{4}}{→}$CH3CHBrCH2Br | |
| B. | CH3CH2OH $→_{170℃}^{浓H_{2}SO_{4}}$ CH2=CH2↑+H2O | |
| C. | CH3COOH+CH3CH2OH $→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH2CH3+H2O | |
| D. | 2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O |
7.下列叙述中正确的是(NA为阿伏加德罗常数)( )
| A. | 1mol Na与足量水反应,转移电子数为NA | |
| B. | 同温同压下,相同体积的物质,其物质的量必相等 | |
| C. | 5.3g Na2CO3固体含有的离子数为1.5NA | |
| D. | 标准状况下,22.4L H2O所含的原子数为3 NA |
11.关于如图所示装置的叙述,不正确的是( )
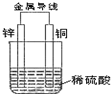

| A. | 铜片上有气泡产生 | B. | 铜片质量逐渐减少 | ||
| C. | 电子从锌片经导线流向铜 | D. | 该装置把化学能转化为电能 |
12.下列措施或事实能用勒夏特列原理解释的是( )
| A. | 新制的氯水在光照下颜色逐渐变浅 | |
| B. | H2、I2、HI平衡混合气缩小体积加压后颜色变深 | |
| C. | 工业上生产硫酸的过程中,SO2在催化氧化时条件控制为常压,而不是高压 | |
| D. | 工业上合成氨气时温度选择450℃左右,而不是常温 |
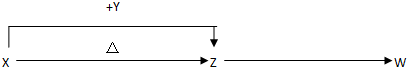
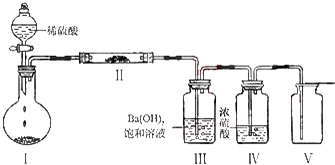
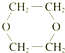 的方案.依次写出合成方案中所涉及反应的化学方程式.
的方案.依次写出合成方案中所涉及反应的化学方程式.