题目内容
过氧化氢(H2O2)可作为采矿业废液消毒剂,如消除采矿废液中剧毒的氰化钾,反应如下:KCN+H2O2+H2O═KHCO3+NH3↑,回答:
(1)H2O2中氧元素的化合价是: .
(2)该反应是否是氧化还原反应? (填“是”或“不是”).其理由是 .
(3)该反应若是氧化还原反应,请回答下列问题;若不是,则不作答.
①被氧化的元素是 ;
②KHCO3 (选填“氧化产物”、“还原产物”,“既是氧化产物,又是还原产物”、“既不是氧化产物,也不是还原产物”)
③若有0.5mol的水参加反应,所转移电子的物质的量是 .
(1)H2O2中氧元素的化合价是:
(2)该反应是否是氧化还原反应?
(3)该反应若是氧化还原反应,请回答下列问题;若不是,则不作答.
①被氧化的元素是
②KHCO3
③若有0.5mol的水参加反应,所转移电子的物质的量是
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)H为+1价,化合物中正负化合价的代数和为0;
(2)C、O元素的化合价变化;
(3)①C元素的化合价由+2价升高为+4价;
②还原剂在反应中被氧化,氧化剂在反应中被还原;
③由反应可知,1molH2O参加反应时,还原剂KCN为1mol,转移电子为1mol×(4-2)=2mol,以此解答.
(2)C、O元素的化合价变化;
(3)①C元素的化合价由+2价升高为+4价;
②还原剂在反应中被氧化,氧化剂在反应中被还原;
③由反应可知,1molH2O参加反应时,还原剂KCN为1mol,转移电子为1mol×(4-2)=2mol,以此解答.
解答:
解:(1)H为+1价,化合物中正负化合价的代数和为0,则H2O2中氧元素的化合价为-1价,故答案为:-1;
(2)因反应前后C、O两元素的化合价发生了改变,则该反应是氧化还原反应,故答案为:是;因为反应前后,C、O两元素的化合价发生了改变;
(3)①C元素的化合价由+2价升高为+4价,则C元素被氧化,故答案为:C;
②还原剂在反应中被氧化,氧化剂在反应中被还原,C、O两元素的化合价发生了改变,则KHCO3既是氧化产物,又是还原产物,
故答案为:既是氧化产物,又是还原产物;
③由反应可知,1molH2O参加反应时,还原剂KCN为1mol,转移电子为1mol×(4-2)=2mol,若有0.5mol的水参加反应,所转移电子的物质的量是0.5mol×2=1mol,
故答案为:1mol.
(2)因反应前后C、O两元素的化合价发生了改变,则该反应是氧化还原反应,故答案为:是;因为反应前后,C、O两元素的化合价发生了改变;
(3)①C元素的化合价由+2价升高为+4价,则C元素被氧化,故答案为:C;
②还原剂在反应中被氧化,氧化剂在反应中被还原,C、O两元素的化合价发生了改变,则KHCO3既是氧化产物,又是还原产物,
故答案为:既是氧化产物,又是还原产物;
③由反应可知,1molH2O参加反应时,还原剂KCN为1mol,转移电子为1mol×(4-2)=2mol,若有0.5mol的水参加反应,所转移电子的物质的量是0.5mol×2=1mol,
故答案为:1mol.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念和转移电子的考查,注意信息及从化合价角度分析,题目难度不大.

练习册系列答案
相关题目
据图判断下列说法不正确的是( )
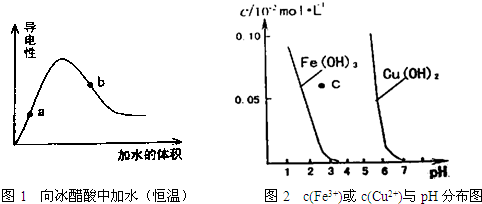

| A、图1中醋酸电离平衡常数:a点的比b点的小 |
| B、图1中醋酸溶液的pH:a点的比b点的大 |
| C、图2中c点对应的溶液为Fe(OH)3的不饱和溶液 |
| D、由图2可知,欲除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调PH约为4左右 |
重金属离子具有毒性.在珠三角某地有甲、乙两个厂排放的重金属离子的废液,甲厂废液经化验主要含有毒的Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低.则乙厂废液中可能含有的离子是( )
| A、Cu2+和SO42- |
| B、Cu2+和Cl- |
| C、K+和SO42- |
| D、Ag+和NO3- |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、标准状况下,11.2L氯仿中含有的C-Cl键的数目为1.5NA |
| B、25℃时,pH=13的Na2CO3溶液中由水电离出的OH-数目为0.1NA |
| C、0.1 mol C12H22O11在一定条件下完全水解生成的葡萄糖分子数目为0.2NA |
| D、4.6 g金属钠与足量氧气反应被氧化成Na2O和Na2O2,生成物中阴离子个数为0.1NA |
室温下,下列叙述正确的是(溶液体积变化忽略不计)( )
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A、在①、②中分别加入氯化铵晶体,两溶液的pH均增大 |
| B、将等体积的③、④分别加水稀释100倍,所得溶液的pH:③<④ |
| C、①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、②、③两溶液混合,若所得溶液的pH=7,则c(CH3COO-)>c(Na+) |
下列化学实验事实相应的离子方程式正确的是( )
| A、往FeCl3溶液中加入Fe粉:2Fe3++Fe═3Fe2+ | ||
| B、往澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2═CaCO3↓+H2O | ||
| C、往FeCl3溶液中加入Cu粉:Fe3++Cu═Fe2++Cu2+ | ||
D、向Ba(OH)2溶液中滴加稀硫酸:Ba2++S
|
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下1molHCl与HF的混合物的体积约为22.4L |
| B、0.5L0.5mol/L的NaNO3溶液中含有的粒子总数约为0.5×6.02×1023 |
| C、常温常压下,1 mol甲基(-CH3)所含的电子数为9NA |
| D、9 g重水所含有的电子数为5NA |