题目内容
A、B、C、D为原子序数依次增大的4种短周期元素.已知:①A、B、C位于同一周期,C、D位于同一主族.A的原子的最外层电子数是其次外层电子数的2倍.②C的某氢化物是最常用的溶剂.请回答:
(1)AC2中具有的化学键的类型是 (填“共价键”或“离子键”).
(2)高温时,6g A的单质与C的常见氢化物(气态)反应,生成两种还原性气体,吸收的热量为65.75kJ,其反应的热化学方程式是 .
(3)C与氢元素可组成含有10个电子的X-,与X-组成元素相同,原子个数比也相同的分子制备C2的化学方程式为 .
(4)将盛有一定量红棕色气体BC2的4L容器压缩至2L,待气体颜色不再变化时,容器内的压强 (填“大于”、“等于”或“小于”)原来的2倍,此过程中容器内气体颜色的变化为 .
(5)DC2与C2可反应生成DC3,写出该反应的化学方程式 .
(1)AC2中具有的化学键的类型是
(2)高温时,6g A的单质与C的常见氢化物(气态)反应,生成两种还原性气体,吸收的热量为65.75kJ,其反应的热化学方程式是
(3)C与氢元素可组成含有10个电子的X-,与X-组成元素相同,原子个数比也相同的分子制备C2的化学方程式为
(4)将盛有一定量红棕色气体BC2的4L容器压缩至2L,待气体颜色不再变化时,容器内的压强
(5)DC2与C2可反应生成DC3,写出该反应的化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D为原子序数依次增大的4种短周期元素.A的原子的最外层电子数是其次外层电子数的2倍,A原子只能有2个电子层,最外层电子数为4,则A为碳元素;A、B、C位于同一周期,C的某氢化物是最常用的溶剂,则C为氧元素;C、D位于同一主族,则D为硫元素;B的原子序数介于碳、氧之间,故B为氮元素,据此解答.
解答:
解:A、B、C、D为原子序数依次增大的4种短周期元素.A的原子的最外层电子数是其次外层电子数的2倍,A原子只能有2个电子层,最外层电子数为4,则A为碳元素;A、B、C位于同一周期,C的某氢化物是最常用的溶剂,则C为氧元素;C、D位于同一主族,则D为硫元素;B的原子序数介于碳、氧之间,故B为氮元素,
(1)AC2为CO2,碳原子与氧原子之间形成共价键,故答案为:共价键;
(2)高温时,6g碳的单质与水(气态)反应生成CO与氢气,吸收的热量为65.75kJ,6g碳的物质的量=
=0.5mol,故1mol碳反应吸收的热量=65.75kJ×
=131.5kJ,故该反应的热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol,
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol;
(3)O元素与氢元素可组成含有10个电子的X-为OH-,与OH-组成元素相同,原子个数比也相同的分子制备O2,为过氧化氢分解生成水与氧气,反应化学方程式为:2H2O2
2H2O2+O2↑,
故答案为:2H2O2
2H2O2+O2↑;
(4)将盛有一定量红棕色气体NO2的4L容器压缩至2L,待气体颜色不再变化时,
由于存在平衡2NO2?N2O4,将4L容器压缩至2L,压强增大,平衡向正反应方向移动,故容器内的压强小于原来的2倍,开始二氧化氮浓度增大,而后平衡向正反应方向移动,二氧化氮浓度减小,故此过程中容器内气体颜色的变化为先变深后变浅,
故答案为:小于;先变深后变浅;
(5)SO2与O2可反应生成SO3,该反应的化学方程式为:2SO2+O2 2SO3,故答案为:2SO2+O2
2SO3,故答案为:2SO2+O2 2SO3.
2SO3.
(1)AC2为CO2,碳原子与氧原子之间形成共价键,故答案为:共价键;
(2)高温时,6g碳的单质与水(气态)反应生成CO与氢气,吸收的热量为65.75kJ,6g碳的物质的量=
| 6g |
| 12g/mol |
| 1mol |
| 0.5mol |
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.5kJ/mol;
(3)O元素与氢元素可组成含有10个电子的X-为OH-,与OH-组成元素相同,原子个数比也相同的分子制备O2,为过氧化氢分解生成水与氧气,反应化学方程式为:2H2O2
| ||
故答案为:2H2O2
| ||
(4)将盛有一定量红棕色气体NO2的4L容器压缩至2L,待气体颜色不再变化时,
由于存在平衡2NO2?N2O4,将4L容器压缩至2L,压强增大,平衡向正反应方向移动,故容器内的压强小于原来的2倍,开始二氧化氮浓度增大,而后平衡向正反应方向移动,二氧化氮浓度减小,故此过程中容器内气体颜色的变化为先变深后变浅,
故答案为:小于;先变深后变浅;
(5)SO2与O2可反应生成SO3,该反应的化学方程式为:2SO2+O2
 2SO3,故答案为:2SO2+O2
2SO3,故答案为:2SO2+O2 2SO3.
2SO3.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,侧重对基础知识的巩固,(4)中注意压缩后颜色虽然先变深后变浅,但仍比原来的颜色深.

练习册系列答案
 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、含1mol Fe(OH)3的胶体中的胶体粒子数目为NA |
| B、1mol氯气与足量的氢氧化钠反应电子转移总数为2NA |
| C、常温下,23g NO2和N2O4的混合气体中含有NA个氧原子 |
| D、11.2L CO2与8.5g NH3所含的分子数相等 |
用于解释下列现象的化学用语表述正确的是( )
| A、硫化钠溶液呈碱性:S2-+2H2O?H2S+2OH- |
| B、亚硫酸溶液呈酸性:H2SO3═2H++SO32- |
| C、氯化铝溶液跟过量的氨水反应:Al3++4OH-═[Al(OH)4]- |
| D、FeCl3溶液呈酸性:Fe3++3H2O?Fe(OH)3+3H+ |
 它可通过不同化学反应分别制得B、C、D和E四种物质.
它可通过不同化学反应分别制得B、C、D和E四种物质.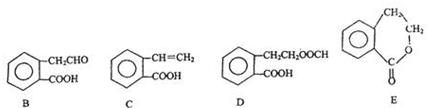
 、HCOOH、CH3COOC2H5
、HCOOH、CH3COOC2H5

 原子序数小于36的X、Y、Z、M、N、W六种元素,原子序数依次增大.已知X是迄今为止形成化合物最多的元素.Y原子最外层电子数与核外电子总数之比为3:4.M元素的常见氧化物有两种,其中一种常温下为气体,且是主要的大气污染物.Z、M、N 同周期,M2-、N-、Z+ 离子半径逐渐减小.W是第Ⅷ族元素中原子序数最小的元素.据此回答:
原子序数小于36的X、Y、Z、M、N、W六种元素,原子序数依次增大.已知X是迄今为止形成化合物最多的元素.Y原子最外层电子数与核外电子总数之比为3:4.M元素的常见氧化物有两种,其中一种常温下为气体,且是主要的大气污染物.Z、M、N 同周期,M2-、N-、Z+ 离子半径逐渐减小.W是第Ⅷ族元素中原子序数最小的元素.据此回答: