题目内容
相对分子质量为72的烷烃,其分子式是 ,若此有机物的一氯代物分子中有两个-CH3、两个-CH2-、一个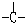 和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式. 、 、 .
和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式. 、 、 .
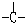 和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式.
和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式.考点:常见有机化合物的结构,有机化合物的异构现象
专题:同分异构体的类型及其判定
分析:先根据烷烃的通式计算写出分子式,然后判断C5H11Cl为戊烷的一氯代物,判断和书写烷烃的一氯代物的异构体可以按照以下步骤来做:先确定烷烃的碳链异构,即烷烃的同分异构体,找出等效的氢原子,根据先中心后两边的原则,将氯原子逐一去代替氢原子,据此判断符合条件的同分异构体数目.
解答:
解:相对分子质量为72的烷烃,烷烃通式为CnH2n+2=72;计算得到n=5,分子式为:C5H12;
戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、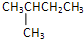 、
、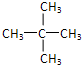 .
.
若为CH3-CH2-CH2-CH2-CH3,一氯代物有:CH3CH2CH2CH2CH2Cl;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;其中CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3符合条件.
若为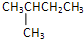 ,一氯代物有:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;其中CH3CH(CH3)CH2CH2Cl;CH2ClCH(CH3)CH2CH3符合条件.
,一氯代物有:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;其中CH3CH(CH3)CH2CH2Cl;CH2ClCH(CH3)CH2CH3符合条件.
若为 ,一氯代物:CH3C(CH3)2CH2Cl,不符合条件.
,一氯代物:CH3C(CH3)2CH2Cl,不符合条件.
故答案为:C5H12;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;CH3CH(CH3)CH2CH2Cl.
戊烷的同分异构体有CH3-CH2-CH2-CH2-CH3、
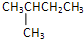 、
、 .
.若为CH3-CH2-CH2-CH2-CH3,一氯代物有:CH3CH2CH2CH2CH2Cl;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;其中CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3符合条件.
若为
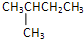 ,一氯代物有:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;其中CH3CH(CH3)CH2CH2Cl;CH2ClCH(CH3)CH2CH3符合条件.
,一氯代物有:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;其中CH3CH(CH3)CH2CH2Cl;CH2ClCH(CH3)CH2CH3符合条件.若为
 ,一氯代物:CH3C(CH3)2CH2Cl,不符合条件.
,一氯代物:CH3C(CH3)2CH2Cl,不符合条件.故答案为:C5H12;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;CH3CH(CH3)CH2CH2Cl.
点评:本题考查了有机化合物的通式应用,同分异构体的分析判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知蓄电池在放电时起原电池的作用,充电时起电解池的作用.铅蓄电池在放电和充电时发生的化学反应可用下式表示:
Pb+PbO2+2H2SO4
2PbSO4+2H2O据此判断下列叙述正确的是( )
Pb+PbO2+2H2SO4
| 放电 |
| 充电 |
| A、放电时负极电极反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| B、充电时阴极电极反应式为:PbSO4+2e-=Pb+SO42- |
| C、充电时,若要使1mol PbSO4转变为Pb和PbO2,则需要通过2mol电子 |
| D、放电时,H+向负极移动 |
在恒温、恒容的条件下,有反应2A(g)+2B(g)?C(g)+3D(g),现从两条途径分别建立平衡.途径Ⅰ:A、B的起始浓度均为2mol/L;途径Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L.则以下叙述不正确的是( )
| A、两途径最终达到平衡时,体系内混合气的平均相对分子质量不同 | ||
| B、两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| C、达平衡时,途径Ⅰ的反应速率v(A)小于途径Ⅱ的反应速率v(A) | ||
D、达平衡时,途径Ⅰ所得混合气的密度为途径Ⅱ所得混合气密度的
|
下列叙述不正确的是( )
| A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B、铜锌原电池工作时,电流沿外电路从铜电极流向锌电极 |
| C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D、为加快锌粒与盐酸反应的速率,可以向溶液中加入几滴氯化铜溶液 |
组成金属单质的微粒( )
| A、金属原子 |
| B、金属阳离子和电子 |
| C、金属原子和电子 |
| D、阳离子和阴离子 |
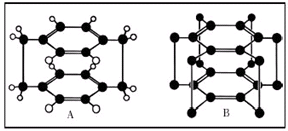
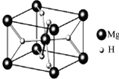 MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度ag?cm-3,则晶胞的体积为
MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度ag?cm-3,则晶胞的体积为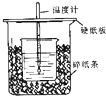 用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: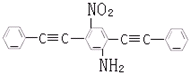
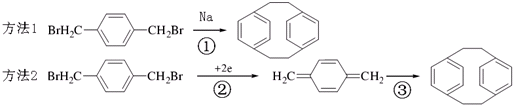 反应①的类型是:
反应①的类型是: