题目内容
9.由苯及丙酮经如下步骤可合成N-异丙基苯胺:
已知(
 )
)①反应条件1所选用的试剂为浓硝酸、浓硫酸,
②反应条件2所选用的试剂为Fe粉/稀盐酸,
③I的结构简式为
 .
.
分析 由苯与浓硝酸、浓硫酸在加热条件下得到H为硝基苯,硝基苯在Fe粉/盐酸条件下还有得到I为 ,再与(CH3)2C=O反应得到J为
,再与(CH3)2C=O反应得到J为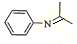 ,最后加成反应还原得到
,最后加成反应还原得到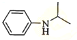 ,以此来解答.
,以此来解答.
解答 解:由苯与浓硝酸、浓硫酸在加热条件下得到H为硝基苯,硝基苯在Fe粉/盐酸条件下还有得到I为 ,再与(CH3)2C=O反应得到J为
,再与(CH3)2C=O反应得到J为 ,最后加成反应还原得到
,最后加成反应还原得到 ,
,
①反应条件1所选用的试剂为浓硝酸、浓硫酸,故答案为:浓硝酸、浓硫酸;
②反应条件2所选用的试剂为Fe粉/稀盐酸,故答案为:Fe粉/稀盐酸;
③I的结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物的合成,为高频考点,把握有机物中官能团变化、有机反应为解答的关键,侧重分析与推断能力的考查,题目难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
14.室温下,CH3COOH的Ka=1.7×10-5mol•L-1,NH3•H2O的Kb=1.7×10-5mol•L-1,下列说法不正确的是( )
| A. | 室温下,相同浓度的CH3COOH与NH3•H20的电离程度相同 | |
| B. | 温度改变后,Ka、Kb都会发生改变 | |
| C. | 室温下,CH3COOH溶液中的[H+]与NH3•H2O中的[OH-]相等 | |
| D. | 室温下,相同物质的量浓度时,CH3COOH溶液中的[H+]与NH3•H2O中的[OH-]相等 |
1.下列分子中每个原子的最外层都满足8电子的是( )
| A. | F2 | B. | H2O | C. | PCl3 | D. | SO2 |
1.下表是某兴趣小组通过实验获得的稀硫酸与某金属反应的实验数据:
分析上述数据,回答下列问题:
(1)上述反应中,反应物的总能量比生成物的总能量高(选填“高”、“低”或“相等”).
(2)实验l、2可得出的结论是反应物浓度越大,反应速率越快;实验3、4可得出的结论是反应温度越高,反应速率越快.
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡.该金属的金属活动性比铁强(选填“强”或“弱”),铁电极上发生的电极反应式为2H++2e-=H2↑.
| 实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | V(H2SO4) mL | 溶液温度/℃ | 金属消失 的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 丝 | 0.7 | 50 | 20 | 35 | 250 |
| 2 | 0.10 | 丝 | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | 丝 | 1.0 | 50 | 20 | 35 | 125 |
| 4 | 0.10 | 丝 | 1.0 | 50 | 35 | 50 | 50 |
(1)上述反应中,反应物的总能量比生成物的总能量高(选填“高”、“低”或“相等”).
(2)实验l、2可得出的结论是反应物浓度越大,反应速率越快;实验3、4可得出的结论是反应温度越高,反应速率越快.
(3)若将该金属与铁用导线连接,插入盛有稀硫酸的烧杯中制作成原电池,观察到铁的表面有大量气泡.该金属的金属活动性比铁强(选填“强”或“弱”),铁电极上发生的电极反应式为2H++2e-=H2↑.
2.分子式为C 8H 10的某有机物,可能属于何种类别( )
| A. | 烷烃 | B. | 烯烃 | C. | 炔烃 | D. | 芳香烃 |
 ,此反应类型为:取代反应.
,此反应类型为:取代反应.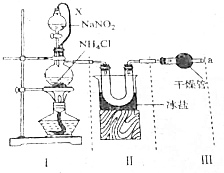 氮气、氨及铵盐用途非常广泛.回答下列问题:
氮气、氨及铵盐用途非常广泛.回答下列问题: