题目内容
15.用18mol•L-1的浓H2SO4配制100mL浓度为1.8mol•L-1的H2SO4,其操作可分为以下各步:a.用量筒量取10.0ml浓H2SO4缓缓注入装有约50mL蒸馏水的烧杯中,并用玻璃棒不断搅拌
b.用约30mL蒸馏水,洗涤烧杯和玻璃棒三次,将每次洗涤液都倒入容量瓶里
c.将稀释后H2SO4冷却到室温后小心转移入容量瓶里
d.检查100mL容量瓶口部是否会发生滴漏
e.将蒸馏水直接加入容量瓶,至液面接近环形刻度线1-2cm处
f.盖紧瓶塞,反复颠倒振荡,摇匀溶液
g.用 向容量瓶里逐滴滴入蒸馏水,至液面最低点恰好和环形刻度线相切填写下列的空白
(1)步骤C中玻璃棒的作用是引流
(2)步骤g中空白处所用仪器名称为胶头滴管
(3)正确的操作顺序是(字母填写)d,a,c,b,e,g,f
(4)该实验中应选择下列那种规格的容量瓶:B
A.150ml B.100ml C.250ml
(5)误差分析,对所配溶液浓度的影响(填偏大,偏小或无影响)
①定容时,俯视刻度线:偏大
②摇匀后液面低于刻度线后又加水:偏小
③配制前,容量瓶壁上有少量水:无影响
④未洗涤烧杯和玻璃棒:偏小.
分析 (1)玻璃棒的作用是搅拌和引流,据实验实际来回答;
(2)根据实验操作步骤选择仪器;
(3)根据浓溶液来配制稀溶液的实验操作步骤来解答;
(4)根据配制溶液的体积选择合适的容量瓶;
(5)依据c=$\frac{n}{V}$分析,凡是使n减小,V偏大的操作都会使溶液的浓度偏小,反之,溶液的浓度偏大.
解答 解:(1)在转移液体的操作中,玻璃棒的作用是引流,故答案为:引流;
(2)定容操作用到的仪器是:胶头滴管,故答案为:胶头滴管;
(3)操作步骤有检查容量瓶是否漏水、量取、稀释、移液、洗涤、定容、摇匀等操作,故正确的顺序为:d,a,c,b,e,g,f;
故答案为:d,a,c,b,e,g,f;
(4)容量瓶只有一条刻度线,只能配制与其规格相同的体积的溶液,配制100mL浓度为1.8mol•L-1的H2SO4,只能选用100ml的容量瓶,故选B;
(5)依据c=$\frac{n}{V}$分析,凡是使n减小,V偏大的操作都会使溶液的浓度偏小,反之,溶液的浓度偏大.
①定容时,俯视读刻度线,导致溶液的体积V偏小,溶液的浓度偏大,故答案为:偏大;
②摇匀后液面低于刻度线后又加水,导致溶液的体积V偏大,溶液的浓度偏小,故答案为:偏小;
③容量瓶中原有少量蒸馏水,对n和V不产生影响,溶液的浓度不变,故答案为:无影响;
④未将所用烧杯洗涤2~3次,会导致溶质损失,则溶液浓度偏小,故答案为:偏小.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
相关题目
5.砹(At)是卤族元素的第五个成员,下列关于砹的叙述不正确的是( )
| A. | 砹位于第六周期第VIIA族 | B. | 砹单质的氧化性比碘强 | ||
| C. | 还原性:At->I- | D. | 稳定性:HAt>HI |
6.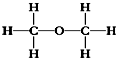 央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )
央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )
 央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )
央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )| A. | 二甲醚和乙醇互为同分异构体且和甲醇互为同系物 | |
| B. | 二甲醚是一种有机物,属于非电解质 | |
| C. | 标准状况下,燃烧11.2L二甲醚一定生成22.4LCO2 | |
| D. | 4.6g该物质中含有共价键的数目为7×6.02×1022 |
3.现有三组溶液:①汽油和氯化钠溶液 ②70%的乙醇溶液 ③氯化钠和单质碘的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸馏、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
10.在强酸性的无色溶液中能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、CO32- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | NH4+、Mg2+、SO42-、Cl- |
20.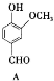 从香荚兰豆中提取的有机物A 用来合成人工香料,其结构简式如图所示.下列关于物质A 的说法正确的是( )
从香荚兰豆中提取的有机物A 用来合成人工香料,其结构简式如图所示.下列关于物质A 的说法正确的是( )
 从香荚兰豆中提取的有机物A 用来合成人工香料,其结构简式如图所示.下列关于物质A 的说法正确的是( )
从香荚兰豆中提取的有机物A 用来合成人工香料,其结构简式如图所示.下列关于物质A 的说法正确的是( )| A. | A 的分子式是C 8H10 O3 | B. | A 分子中含有酯基 | ||
| C. | A 只能发生取代反应 | D. | A 能与NaOH 溶液反应 |
7.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2 L氧气所含的原子数为NA | |
| B. | 含NA个H2SO4分子的浓硫酸与足量铜反应可制得0.5mol SO2 | |
| C. | 15.6 g Na2O2与过量CO2反应时,转移的电子数为0.2NA | |
| D. | 标准状况下,0.5mol NO和0.5mol O2组成的混合气体,体积约为22.4L |