题目内容
(10分)(1)通过NOx传感器可监测NOx的含量,固体体电解质可以传导O2-其工作原理示意图如下:
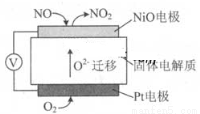
①Pt电极上发生的是 反应(填“氧化”或“还原”)。
②写出NiO电极的电极反应式: 。
(2)一定条件下,如图所示装置可实现有机物的电化学储氢(忽略其他有机物)。
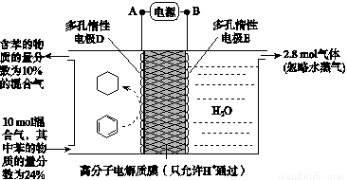
①导线中电子移动方向为________。(用A、D表示)
②生成目标产物的电极反应式为__________________。
③该储氢装置的电流效率η=____________________。(η= ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)
(1)①、还原;②、NO+O2--2e-=NO2 ;(2)①A→D ; ②C6H6+6H++6e-==C6H12 ; ③64.3%
【解析】
试题分析:(1)①在Pt电极上O2得到电子,被还原,发生还原反应变为O2-;②在NiO电极上NO失去电子,被氧化为NO2,该电极反应式是NO+O2--2e-=NO2 ;(2) ①根据图示可知在左边苯在D上得到电子被还原为环己烷,所以A电极电子多,故导线中电子移动方向为A→D ;②生成目标产物的电极反应式为C6H6+6H++6e-==C6H12 ;③在右侧阳极OH-失去电子变为氧气,每转移4mol的电子,会产生1mol的氧气,现在产生氧气的物质的量是2.8mol,所以转移电子的物质的量是2.8mol×4=11.2mol;每产生1mol的氧气,会同时产生氢气2mol,则产生2.8mol的氧气的同时还在阴极产生了5.6mol的氢气。假设发生反应消耗的苯的物质的量是xmol,反应消耗氢气的物质的量是3xmol;剩余苯的物质的量是10mol×24%-x,由于反应后苯的含量是:(10mol×24%-x)÷(10-3x+5.6)=10%,解得x=1.2mol,则消耗的电子的物质的量是6×1.2mol=7.2mol,所以该储氢装置的电流效率η=(7.2mol÷11.2mol)× 100% =64.3%。
考点:考查原电池、电解池的反应原理、电极反应及物质的转化效率的知识。

 全能练考卷系列答案
全能练考卷系列答案在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下进行反应,一段时间后测得反应前后各物质质量如右表: 则该密闭容器中发生化学反应的基本类型可能是( )
则该密闭容器中发生化学反应的基本类型可能是( )
物质 | X | Y | Z | Q |
反应前质量/g | 20 | 20 | 20 | 20 |
反应后质量/g | 20 | 30 | 16 | 14 |
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数 (25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项错误的是
A.HCN+CO32- = CN-+ HCO3-
B.2HCOOH+CO32- = 2HCOO-+H2O+CO2↑
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
 H++OH- △H>0。下列叙述正确的是
H++OH- △H>0。下列叙述正确的是 2Fe+3CO2
2Fe+3CO2 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑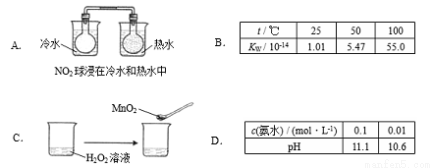
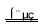 2OH- +Cl2↑ +H2↑
2OH- +Cl2↑ +H2↑