题目内容
4.在标准状况下,气体摩尔体积约为22.4L/mol,则标准状况下0.5mol水的体积约为( )| A. | 0.5L | B. | 5L | C. | 11.2L | D. | 不能确定 |
分析 标况下水为液态,不能根据气体摩尔体积来计算.
解答 解:气体摩尔体积只适用于气体,而标况下水为液态,不能根据气体摩尔体积来计算其体积,故选D.
点评 本题考查了气体摩尔体积的适用对象,难度不大,应注意的是气体摩尔体积只适用于气体.

练习册系列答案
相关题目
14.下列关于物质或离子检验的叙述正确的是( )
| A. | 向某溶液中加入BaCl2溶液,出现白色沉淀,再加稀硝酸溶液,若沉淀不溶解,则该溶液中肯定有SO42- | |
| B. | 灼烧某白色粉末,火焰呈黄色,则证明原粉末中肯定有Na+,无K+ | |
| C. | 向某溶液中滴加AgNO3溶液后,出现白色沉淀,再加稀盐酸,若沉淀不溶解,则证明溶液中肯定有Cl- | |
| D. | 在某盐溶液中加入氢氧化钠浓溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,则该溶液中肯定有NH4+ |
15.阿司匹林的结构简式如图,把阿司匹林放在足量的氢氧化钠溶液中煮沸,能发生反应的化学键是( )


| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
9.关于反应方程式Cl2+2I-═2Cl-+I2,说法不正确的是( )
| A. | Cl2是氧化剂 | B. | I2是还原产物 | ||
| C. | 上述反应属于置换反应 | D. | 上述反应属于离子反应 |
16.已知苹果酸的结构简式为: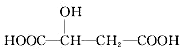 下列说法正确的是( )
下列说法正确的是( )
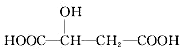 下列说法正确的是( )
下列说法正确的是( )| A. | 苹果酸分子中存在5种不同种类的氢原子 | |
| B. | 1mol苹果酸可与3mol NaOH完全中和 | |
| C. | 苹果酸与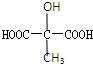 互为同分异构体 互为同分异构体 | |
| D. | 苹果酸分子中的所有碳原子可能处在同一条直线上 |
13.一定条件下,体积为1L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
| A. | 以X浓度变化表示的反应速率为0.01mol•L-1•S-1 | |
| B. | 将容器体积变为2L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H>0 |
14.如图为铜丝与浓硫酸反应并验证其产物性质的实验装置.
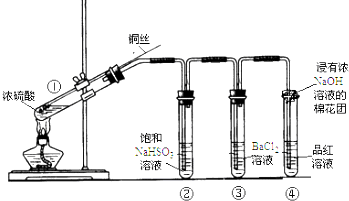
(1)①中反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)②中饱和NaHSO3溶液的作用是除去除去①中挥发出的硫酸.加热一段时间后,③中溶液依然澄清,想要立即终止铜与硫酸的反应,最恰当的方法是a.
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
完成上述反应的离子方程式.
(4)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色.取少量蓝色溶液于试管中,滴加NaOH溶液过量,出现的现象是开始没有明显现象,后有蓝色沉淀生成.

(1)①中反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)②中饱和NaHSO3溶液的作用是除去除去①中挥发出的硫酸.加热一段时间后,③中溶液依然澄清,想要立即终止铜与硫酸的反应,最恰当的方法是a.
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
| 加入试剂 | 现象 | 反应的离子方程式 | |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | SO2+2OH-═SO32-+H2OBa2++SO32-═BaSO3↓ |
| 第二份 | 加入氯水 | 有白色沉淀生成 | SO2+Cl2+H2O═4H++2Cl-+SO42-Ba2++SO42-═BaSO4↓ |
(4)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色.取少量蓝色溶液于试管中,滴加NaOH溶液过量,出现的现象是开始没有明显现象,后有蓝色沉淀生成.