题目内容
2.某课外小组设计实验制取乙酸乙酯的装置如图所示,下列说法正确的是( )(填选项字母)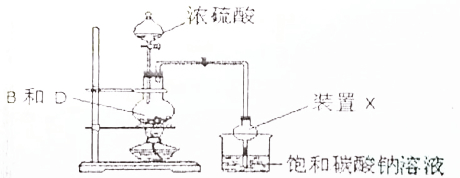
| A. | 反应中浓硫酸的作用是催化剂、吸水剂 | |
| B. | 饱和碳酸钠溶液可用饱和氢氧化钠溶液代替 | |
| C. | 实验结束后烧杯中的溶液经震荡、静置、分液,能得到纯净的乙酸乙酯 | |
| D. | 装置X的作用能防止倒吸 |
分析 乙酸和乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯,乙酸乙酯中混有乙酸、乙醇,用X装置可防止倒吸,因乙酸乙酯不溶于饱和碳酸钠溶液,且乙酸可与碳酸钠溶液反应,可用饱和碳酸钠溶液吸收,以此解答该题.
解答 解:A.反应为可逆反应,浓硫酸的作用是催化剂,因生成水,浓硫酸还起到吸水剂的作用,有利于平衡正向移动,故A正确;
B.乙酸乙酯在氢氧化钠溶液中发生水解,不能用氢氧化钠,故B错误;
C.乙醇易溶于乙酸乙酯,则实验结束后烧杯中的溶液经振荡、静置、分液,不能得到纯净的乙酸乙酯,故C错误;
D.因生成乙酸、乙醇易溶于水,则装置X的作用是能防止倒吸,故D正确.
故选AD.
点评 本题考查乙酸乙酯的制备,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的原理、操作方法,难度不大.

练习册系列答案
相关题目
14.室温下,分别用0.1mol•L-1下列溶液进行实验,结论不正确的是( )
| A. | 向CH3COONa溶液中加入盐酸至pH=7:c(Na+)=c(Cl-)+c(CH3COO-) | |
| B. | 向NaHCO3中滴入NaOH溶液至反应完全:c(Na+)=2[c(HCO3-)+c(CO32-)+c(H2CO3)] | |
| C. | 向氨水中加入少量NH4Cl固体:$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| D. | 向NaHSO4溶液中加入等浓度等体积的Ba(OH)2溶液:pH=13 |
15.下列金属表面可自然形成致密氧化膜的是( )
| A. | K | B. | Na | C. | Fe | D. | Al |
12.下列化工生产过程中,未涉及氧化还原反应的是( )
| A. | 侯式制碱法制纯碱 | B. | 海带提碘 | ||
| C. | 氯碱工业 | D. | 海水提溴 |
11.下列关于物质的量浓度表述正确的是( )
| A. | 0.3mol•L-1 的Na2SO4溶液中含有Na+和SO42-的总物质的量为0.9mol | |
| B. | 当1L水吸收22.4L氨气时所得氨水的浓度不是1mol•L-1,只有当22.4L氨气溶于水制得1L氨水时,其浓度是1mol•L-1 | |
| C. | 在K2SO4和NaCl的混合溶液中,如果Na+和SO42-的物质的量相等,则K+和Cl-的物质的量浓度一定相同 | |
| D. | 250g胆矾溶于水得到1L溶液,所得CuSO4溶液的物质的量浓度为1mol•L-1 |
12.在强酸性溶液中能大量共存的无色透明离子组是( )
| A. | K+、Na+、NO3-、MnO4- | B. | K+、Na+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、Cu2+ | D. | Na+、Ba2+、OH-、SO42- |