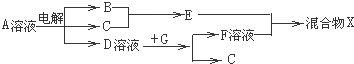
题目内容
下列说法错误的是( )
| A、0.1 mol?L-1的CH3COOH溶液中,由水电离的[H+]为10-13mol?L-1 |
| B、pH=2与pH=1的CH3COOH溶液中[H+]之比为1:10 |
| C、pH=12的NaOH溶液和pH=2的CH3COOH溶液等体积混合,混合后溶液pH<7 |
| D、1 mol醋酸分子中含有共价键的个数为8NA |
考点:弱电解质在水溶液中的电离平衡,物质结构中的化学键数目计算,酸碱混合时的定性判断及有关ph的计算
专题:
分析:A、CH3COOH是弱电解质,部分电离,不知道溶液的PH,无法求算溶液中的c(H+);
B、pH=2,c(H+)=10-2,PH=1,c(H+)=10-1;
C、CH3COOH是弱电解质,部分电离,c(CH3COOH)远远大于10-2;
D、CH3COOH中含有三个C-H键、一个C═O双键,一个C-C键、一个C-O键、一个O-H键.
B、pH=2,c(H+)=10-2,PH=1,c(H+)=10-1;
C、CH3COOH是弱电解质,部分电离,c(CH3COOH)远远大于10-2;
D、CH3COOH中含有三个C-H键、一个C═O双键,一个C-C键、一个C-O键、一个O-H键.
解答:
解:A、CH3COOH属于弱电解质,溶液中部分电离,题中没有溶液的PH,无法求算溶液中的c(H+),故A错误;
B、CH3COOH溶液的pH=2,则c(H+)=10-2mol/L,PH=1,c(H+)=10-1mol/L,两溶液中c(H+)之比为1:10,故B正确;
C、由于CH3COOH是弱电解质,溶液中部分电离,c(CH3COOH)远远大于10-2mol/L,与氢氧化钠反应后醋酸大量剩余,溶液显示酸性,PH<7,故B正确;
D、在CH3COOH分子中,共含有三个C-H键、一个C═O双键,一个C-C键、一个C-O键、一个O-H键,总计8个共价键,1mol醋酸分子中含有共价键的个数为8NA,故D正确.
故选A.
B、CH3COOH溶液的pH=2,则c(H+)=10-2mol/L,PH=1,c(H+)=10-1mol/L,两溶液中c(H+)之比为1:10,故B正确;
C、由于CH3COOH是弱电解质,溶液中部分电离,c(CH3COOH)远远大于10-2mol/L,与氢氧化钠反应后醋酸大量剩余,溶液显示酸性,PH<7,故B正确;
D、在CH3COOH分子中,共含有三个C-H键、一个C═O双键,一个C-C键、一个C-O键、一个O-H键,总计8个共价键,1mol醋酸分子中含有共价键的个数为8NA,故D正确.
故选A.
点评:本题考查的是弱电解质在水溶液中的电离平衡,难度不大,关键看清题干要求.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
下列关于同分异构体、同系物、同素异形体、同位素的说法中错误的是( )
| A、乙酸与甲酸甲酯互为同分异构体 | ||||
B、
| ||||
| C、氧气与臭氧互为同素异形体 | ||||
| D、乙烯与聚乙烯互为同系物 |
下列反应的离子方程式书写正确的是( )
| A、铝与稀硫酸反应:Al+2H+=Al3++H2↑ |
| B、碳酸钙与稀盐酸的反应:CO32-+2H+=CO2+H2O |
| C、氨水与盐酸反应:OH-+H+=H2O |
| D、实验室用氢氧化钠溶液吸收多余的Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
下列说法正确的是( )
| A、油脂水解可得到高级脂肪酸和甘油 |
| B、糖类都是溶于水、有甜味的物质 |
| C、有机物大多数都能燃烧 |
| D、所有糖都能水解 |
化学平衡常数K的数值大小是衡量化学反应进行程度的标志.在常温下,下列反应的平衡常数的数值如下:以下说法正确的是( )
2NO(g)?N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g)?2H2O(l) K2=2×1081
2CO2(g)?2CO(g)+O2(g) K3=4×10-92.
2NO(g)?N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g)?2H2O(l) K2=2×1081
2CO2(g)?2CO(g)+O2(g) K3=4×10-92.
| A、常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)?c(O2) |
| B、常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C、常温下,NO、H2O、CO2三种化合物分解放出O2的倾向由大到小的顺序为NO>H2O>CO2 |
| D、以上说法都不正确 |
甲、乙两物质的溶解度曲线如图所示,下列说法正确的是( )
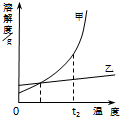

| A、t1℃时,物质的量浓度:甲=乙 |
| B、温度变化相同时,溶解度数值的变化量:甲>乙 |
| C、t2℃时,饱和溶液中溶质的质量分数:甲=乙 |
| D、相同质量的饱和溶液由t2℃降到t1℃时,析出的固体:甲<乙 |
下列溶液在空气中加热、蒸干、灼烧后,所得固体为原溶液中的溶质的是( )
| A、(NH4)2SO3 |
| B、KMnO4 |
| C、AlCl3 |
| D、Na2CO3 |