题目内容
4.下列化学用语或模型不正确的是( )| A. | 甲烷分子的比例模型: | B. | 氯化氢的电子式:H:Cl | ||
| C. | 乙烷的分子式:C2H6 | D. | 乙烯的结构简式:CH2=CH2 |
分析 A、比例模型体现的是组成该分子的原子间的大小以及分子的空间结构,且碳原子半径大于氢原子;
B、氯化氢为共价化合物,氯离子最外层应该为8个电子;
C、表示物质的元素组成的式子为分子式;
D、烯烃中的碳碳双键不能省略.
解答 解:A、甲烷为正四面体结构,碳原子半径大于氢离子,甲烷分子的比例模型为: ,故A正确;
,故A正确;
B、氯化氢为共价化合物,氯原子最外层达到8个电子稳定结构,氯化氢的电子式为: ,故B错误;
,故B错误;
C、表示物质的元素组成的式子为分子式,故乙烷的分子式为C2H6,故C正确;
D、烯烃中的碳碳双键不能省略,故乙烯的结构简式为CH2=CH2,故D正确.
故选B.
点评 本题考查了电子式、比例模型和分子式、结构简式的书写,题目难度中等,注意掌握常见化学用语的概念及表示方法,明确离子化合物和共价化合物的电子式的区别.

练习册系列答案
相关题目
14.设NA表示阿伏加德罗常数值,下列叙述正确的是( )
| A. | NA个氧气分子和NA个氢气分子的质量比为16:1 | |
| B. | 54g H2O中含有的水分子数为3NA个 | |
| C. | 11.2L 氯气中含有的原子数为NA个 | |
| D. | 2L 1mol/L Na2SO4溶液中Na+离子数为2NA个 |
12.把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀,该混合溶液中钾离子浓度为( )
| A. | 10 (b-2a)mol•L-1 | B. | 5(b-2a)mol•L-1 | C. | 2(b-a)mol•L-1 | D. | 10(2a-b)mol•L-1 |
19.下列操作不能说明仪器组装气密性良好的是( )
| A. | 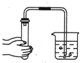 | B. | 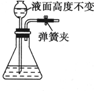 | C. | 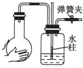 | D. |  |
9.能正确表示下列反应的离子方程式是( )
| A. | 金属铝溶于稀硫酸中:Al+2H+═A13++H2↑ | |
| B. | 少量Cl2通入KI溶液中:Cl2+2I-═2C1-+I2 | |
| C. | 醋酸钠水溶液中通入足量CO2:2CH3COO-+CO2+H2O═2CH3COOH+CO32- | |
| D. | 碳酸锌溶于稀硝酸中:CO32-+2H+═H2O+CO2↑ |
16.下列电子式书写错误的是( )
| A. | 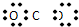 | B. |  | C. | 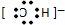 | D. | 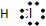 |

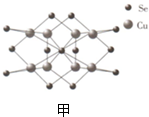

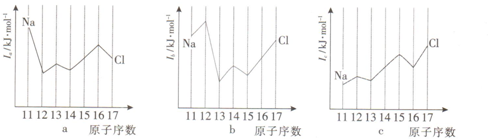
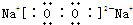 ,其中含有的化学键类型为离子键、非极性键
,其中含有的化学键类型为离子键、非极性键