题目内容
下列各物质中所含有的分子数最多的是( )
| A、标准状况下11.2 L氯气 |
| B、17g氨气(NH3) |
| C、1.204×1024个H2O分子 |
| D、0.8mol氧气 |
考点:物质的量的相关计算
专题:计算题
分析:根据n=
=
=
计算氯气、氨气、水的物质的量,由N=nNA可知,物质的量越大含有分子数目越多.
| V |
| Vm |
| m |
| M |
| N |
| NA |
解答:
解:标况下,11.2L氯气为
=0.5mol,
17g氨气物质的量为
=1mol,
1.204×1024个H2O分子物质的量为
=2mol,
氧气为0.8mol,
故水的物质的量最大,则水分子数目最多,
故选C.
| 11.2L |
| 22.4L/mol |
17g氨气物质的量为
| 17g |
| 17g/mol |
1.204×1024个H2O分子物质的量为
| 1.024×1024 |
| 6.02×1023mol-1 |
氧气为0.8mol,
故水的物质的量最大,则水分子数目最多,
故选C.
点评:本题考查物质的量有关计算,侧重微粒数目的计算,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
某化学兴趣小组把少量废铁屑溶于过量稀硫酸中,过滤,除去杂质,在滤液中加入适量硝酸,再加入过量的氨水,有红褐色沉淀A生成.再过滤,加热至恒重得到B.对物质A、B该小组有如下四种判断,你认为正确的是( )
| A、Fe(OH)3; Fe2O3 |
| B、Fe(OH)2; FeO |
| C、Fe(OH)3、Fe(OH)2;Fe3O4 |
| D、Fe2O3;Fe(OH)3 |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
| B、在非标准状况下,1mol任何气体的体积不可能是22.4L |
| C、标准状况下,22.4L酒精(CH3CH2OH)的分子数为NA |
| D、一定条件下,2.3g的Na完全与O2反应失去的电子数为0.1NA |
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ?mol-1,测得0到10秒内,c(H2)减小了0.75mol?L-1,下列说法正确的是( )
| A、10到15秒内c(NH3) 增加量等于0.25mol?L-1 |
| B、化学反应速率关系是:3υ正(H2)=2υ正(NH3) |
| C、达平衡后,分离出少量NH3,V正增大 |
| D、该反应的逆反应的活化能不小于92.2kJ?mol-1 |
关于氢键,下列说法正确的是( )
| A、氢键属于共价键 |
B、因为分子间存在氢键的缘故,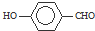 比 比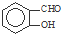 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、1mol冰中有4mol氢键 |
表示下列用途或变化的离子方程式不正确的是( )
| A、泡沫灭火器灭火原理:Al3++3HCO3-=3CO2↑+Al(OH)3↓ |
| B、纯碱代替洗涤剂洗涤餐具:CO32-+H2O?HCO3-+OH- |
| C、明矾净水原理:Al3++3H2O?Al(OH)3+3H+ |
| D、NaHCO3的水解:HCO3-+H2O?H3O++CO32- |
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是( )
| A、1.0mol?L-1的HNO3溶液:NH4+、[Ag(NH3)2]+、Cl-、SO42- |
| B、c(H+)/c(OH-)=10-11的溶液:Na+、Ba2+、NO3-、Cl- |
| C、滴入酚酞显红色的溶液:Ca2+、Al3+、NO3-、HCO3- |
| D、滴入碘化钾淀粉溶液显蓝色的溶液:Na+、Fe2+、ClO-、SO42- |
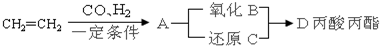
 某有机物A由C、H、O三种元素组成,在一定条件下有如下转化关系,己知在相同条件下,C的蒸气密度是氢气的22倍,并可以发生银镜反应.
某有机物A由C、H、O三种元素组成,在一定条件下有如下转化关系,己知在相同条件下,C的蒸气密度是氢气的22倍,并可以发生银镜反应.