题目内容
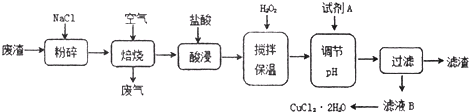
工业上为了处理含有Cr2![]() 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准,请回答下列问题:
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬的含量已低于排放标准,请回答下列问题:
(1)写出两极上的电极反应式:阳极:________;阴极:________.
(2)写出Cr2![]() 变成Cr3+的离子方程式________.
变成Cr3+的离子方程式________.
(3)工业废水由酸性变为碱性的原因是____________________.
(4)能否改用石墨电极?________,原因是________________.
答案:
解析:
解析:
|
答案:(1)Fe-2e- (2)Cr2 (3)因为H+不断放电,打破了水的电离平衡,使溶液中c(OH-)>c(H+),所以溶液由酸性变为碱性 (4)不能改用石墨.因为用石墨作电极,阳极产生氯气,得不到Fe2+,缺少还原剂,不能使Cr2 解析:分析题目可知以Fe为电极电解,则Fe在阳极溶解,其电极反应阳极:Fe-2e- |

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
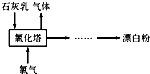 氯气是重要的化工原料.
氯气是重要的化工原料.