题目内容
用实验确定某酸HA是弱电解质.两同学的方法是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸、分别配制pH=1的两种酸溶液各100 mL;
②分别取两种溶液各10 mL,加水稀释为100 mL;
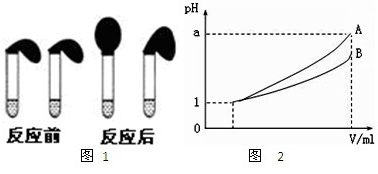
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是________.
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH________1(选填“>”、“<”或“=”).
乙方案中,说明HA是弱电解质的现象是________(多选扣分)
a.装HCl溶液的试管中放出H2的速率快;
b.装HA溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快.
(3)请你评价:乙方案中难以实现之处和不妥之处.
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述.
解析:
|
答案:(1)100 mL容量瓶;(2)>,b;(3)配制pH=1的HA溶液难以实现;不妥之处在于锌粒的表面积不可能完全相同. 思路与技巧:(1)配制一定物质的量浓度的溶液所必需的定量仪器是容量瓶. (2)甲方案中,0.1 mol/L的某弱酸HA,由于它部分电离,H+浓度小于0.1 mol/L,pH应该大于1.乙方案中,在两种稀释液中同时加入浓度相同的锌粒,盐酸稀释体积变大,但H+的物质的量不会增加,pH变化较大.弱酸HA稀释体积也变大,弱酸稀释后,电离度变大,H+的物质的量也增加,因此,pH变化较小.加入锌粒后,装HA溶液的试管中因H+的物质的量浓度大,所以放出H2的速率快. (3)乙方案中,要求配制某一定pH的弱酸溶液,但影响溶液pH的因素很多,如温度变化等,导致配制的溶液的pH不稳定.因此配制pH=1的弱酸溶液难以实现.不妥之处,因为是液体与固体反应,固体的表面积对反应速率的影响大,仅仅用反应产生气体的速率来判断溶液中H+浓度的大小,说服力不强. (4)要证明某酸是弱酸还有很多方法.如:配制NaA的盐溶液,再测量溶液的pH,pH>7,说明HA是弱酸. |

 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案 甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下:
甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动.实验方案如下: