题目内容
下列各组中的物质相互反应时,若两种试剂的量发生改变,不可用同一个离子方程式表示的是( )
| A、氯化铝和氨水 |
| B、硫酸钠和氢氧化钡 |
| C、碳酸氢钙和氢氧化钠 |
| D、碳酸氢钠溶液和盐酸 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氯化铝和氨水反应生成氢氧化铝和氯化铵,与反应物的量无关;
B.硫酸钠和氢氧化钡反应生成硫酸钡和氢氧化钠,与反应物的量无关;
C.碳酸氢钙和少量氢氧化钠反应生成碳酸钙和碳酸氢钠,氢氧化钠足量,反应生成碳酸钙、碳酸钠和水;
D.碳酸氢钠溶液和盐酸反应生成氯化钠、水和二氧化碳,与反应物的用量无关.
B.硫酸钠和氢氧化钡反应生成硫酸钡和氢氧化钠,与反应物的量无关;
C.碳酸氢钙和少量氢氧化钠反应生成碳酸钙和碳酸氢钠,氢氧化钠足量,反应生成碳酸钙、碳酸钠和水;
D.碳酸氢钠溶液和盐酸反应生成氯化钠、水和二氧化碳,与反应物的用量无关.
解答:
解:A.氯化铝和氨水反应的离子方程式:Al3++3NH3?H2O═Al(OH)3 ↓+3NH4+,故A不选;
B.硫酸钠和氢氧化钡反应的离子方程式:Ba2++SO42-=BaSO4↓,故B不选;
C.碳酸氢钙和少量氢氧化钠反应离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H20;碳酸氢钙和过量氢氧化钠反应离子方程式为:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H20,故C选;
D.碳酸氢钠溶液和盐酸反应的离子方程式:H++HCO3-=H2O+CO2↑,故D不选;
故选:C.
B.硫酸钠和氢氧化钡反应的离子方程式:Ba2++SO42-=BaSO4↓,故B不选;
C.碳酸氢钙和少量氢氧化钠反应离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H20;碳酸氢钙和过量氢氧化钠反应离子方程式为:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H20,故C选;
D.碳酸氢钠溶液和盐酸反应的离子方程式:H++HCO3-=H2O+CO2↑,故D不选;
故选:C.
点评:本题考查离子反应方程式的书写,明确发生的反应是解答本题的关键,题目难度不大,熟悉离子反应的书写方法即可解答,注意反应物用量对反应的影响.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
分类法在化学学科发展中起到了非常重要作用.下列分类标准合理的是( )
①根据氧化物的组成元素将氧化物分成酸性氧化物、碱性氧化物等
②根据酸分子中含氢原子的个数将酸分为一元酸、二元酸、三元酸
③根据分散质粒子直径的大小将分散系分为溶液、胶体、浊液
④根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素.
①根据氧化物的组成元素将氧化物分成酸性氧化物、碱性氧化物等
②根据酸分子中含氢原子的个数将酸分为一元酸、二元酸、三元酸
③根据分散质粒子直径的大小将分散系分为溶液、胶体、浊液
④根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素.
| A、③ | B、①③ | C、②③ | D、①②③④ |
下列离子方程式中正确的是( )
| A、NH4HSO4溶液中加入少量NaOH稀溶液:NH4++OH-→NH3?H2O |
| B、Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O→HClO+HSO3- |
| C、酸性高锰酸钾溶液中滴入少量过氧化氢:2MnO4-+7H2O2+6H+→2Mn2++6O2↑+10H2O |
| D、向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
下列离子方程式中正确的是( )
| A、硫化亚铁放入盐酸中:S2-+2 H+→H2S↑ |
| B、硫酸铜溶液中通入硫化氢:Cu2++H2S=CuS↓+2H+ |
| C、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O→AlO2-+4NH4++2H2O |
| D、过量铁粉与氯化铁溶液反应,溶液变浅绿色:Fe+Fe3+→2Fe2+ |
对于胃溃疡较重的病人,不适合使用的抑酸剂是( )
| A、氢氧化镁 |
| B、氢氧化铝 |
| C、碳酸氢钠 |
| D、Na3C6H5O7﹒2H2O |
R元素的一种粒子的结构示意图为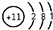 ,则下列说法不正确的是( )
,则下列说法不正确的是( )
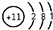 ,则下列说法不正确的是( )
,则下列说法不正确的是( )| A、该粒子容易得电子 |
| B、该粒子的核外有3个电子层 |
| C、R元素为金属元素 |
| D、R元素的原子有11个电子 |
用10ml 0.1mol/L的AgNO3溶液恰好与相同体积的NaCl、MgCl2和AlCl3三种溶液完全反应,则这三种盐酸盐溶液的物质的量浓度之比是( )
| A、3:2:2 |
| B、6:3:2 |
| C、1:3:3 |
| D、3:1:1 |
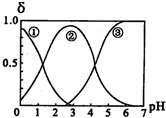 在H2C2O4(草酸)水溶液中,H2C2O4、HC2O4-和C2O42-三种形态的炷子的分布分数δ随溶液pH变化的关系如图所示[已知KSP(CaC2O4)=2.3×10-9].下列说法正确的是( )
在H2C2O4(草酸)水溶液中,H2C2O4、HC2O4-和C2O42-三种形态的炷子的分布分数δ随溶液pH变化的关系如图所示[已知KSP(CaC2O4)=2.3×10-9].下列说法正确的是( )| A、曲线①代表的粒子是HC2O4- |
| B、pH=5时,溶液中:c(C2O42-)>c(H2C2O4)>c(HC2O4-) |
| C、0.1mol?L-1 NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) |
| D、一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)减小,c(Ca2+)不变 |