题目内容
14.下列说法正确的是( )| A. | 浓H2SO4有脱水性,因而可作干燥剂 | |
| B. | 常温下,浓H2SO4可用铝制密闭容器储运 | |
| C. | 浓H2SO4具有氧化性,稀H2SO4无氧化性 | |
| D. | 浓H2SO4难挥发,因而可在敞口容器中储存 |
分析 A、浓H2SO4干燥剂是吸水性;
B、铝与浓硫酸发生钝化;
C、稀硫酸中氢离子表现氧化性;
D、浓硫酸具有吸水性.
解答 解:A、浓H2SO4干燥剂是吸水性,而不脱水性,故A 错误;
B、铝与浓硫酸发生钝化,表面形成致密的氧化膜,所以常温下,浓H2SO4可用铝制密闭容器储运,故B正确;
C、稀硫酸中氢离子表现氧化性,故C错误;
D、浓硫酸具有吸水性,溶液浓度变稀,浓H2SO4不可在敞口容器中储存,故D错误;
故选B.
点评 本题考查了浓硫酸的性质,题目难度不大,明确浓硫酸的特性是解题的关键,注意铝与浓硫酸发生钝化现象.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
4.下列叙述正确的是( )
| A. | 除去FeCl3溶液中的FeCl2杂质可以向该溶液中加入过量的铁粉 | |
| B. | 过量的Fe与Cl2反应,一定生成FeCl3 | |
| C. | Fe3O4可用于生产红色油漆或红色涂料 | |
| D. | 普通钢铁是合金,不锈钢是特种钢,不是合金 |
5.下列溶液中各微粒的浓度关系不正确的是( )
| A. | 0.1 mol/LCH3COOH溶液中:c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | 将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) | |
| C. | CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | Na2S溶液中:c(Na+)=2(c(S2-)+c(HS-)+c(H2S)) |
2.日常生活中使用的购物袋的材料多为聚乙烯,下列说法中正确的是( )
| A. | 用纯净的乙烯合成的聚乙烯是纯净物 | |
| B. | 聚乙烯可以人工合成,也可以是天然高分子化合物 | |
| C. | 聚乙烯能使酸性高锰酸钾溶液褪色 | |
| D. | 聚乙烯的单体能够使溴的四氯化碳溶液褪色 |
9.油脂皂化后,使肥皂和甘油充分分离,可以采用( )
| A. | 萃取 | B. | 蒸馏 | C. | 过滤 | D. | 盐析 |
6.某元素的一种同位素X原子的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX分子中含电子的物质的量是( )
| A. | $\frac{a}{A+m}$(A-N+m)mol | B. | $\frac{a}{A}$(A-N)mol | C. | $\frac{a}{A+m}$(A-N)mol | D. | $\frac{a}{A}$(A-N+m)mol |
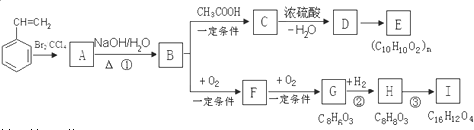
 .
.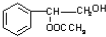 或
或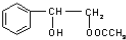 .
.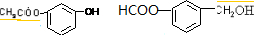 .
. .
.