题目内容
(1)写出下列物质的电子式
①H2 ②NH3 ③NaOH
(2)写出下列物质的结构式①甲烷 ②乙炔
(3)画出质量数为23,中子数为12的原子的原子结构示意图: .
①H2
(2)写出下列物质的结构式①甲烷
(3)画出质量数为23,中子数为12的原子的原子结构示意图:
考点:电子式,原子结构示意图,结构式
专题:化学用语专题
分析:(1)先判断混合物类型,然后根据离子化合物、共价化合物的电子式的表示方法写出各物质的电子式;
(2)甲烷为在说明体积结构,分子中存在4个碳氢键;乙炔为直线型结构,分子中存在一个碳碳三键;
(3)该元素的质子数=质量数-中子数=11,为钠元素,画出钠元素的原子结构示意图.
(2)甲烷为在说明体积结构,分子中存在4个碳氢键;乙炔为直线型结构,分子中存在一个碳碳三键;
(3)该元素的质子数=质量数-中子数=11,为钠元素,画出钠元素的原子结构示意图.
解答:
解:(1)①氢气分子中存在一个H-H共价键,氢气的电子式为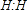 ,故答案为:
,故答案为: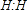 ;
;
②氨气分子中存在3个氮氢键,氮原子最外层达到8个电子稳定结构,氨气的电子式为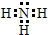 ,故答案为:
,故答案为: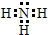 ;
;
③NaOH中钠离子与氢氧根离子之间通过离子键结合,氧原子与氢原子之间存在H-O键,电子式为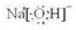 ,故答案为:
,故答案为: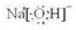 ;
;
(2)①甲烷是碳原子和氢原子间通过共价单键形成的空间正四面体结构,结构式为: ,
,
故答案为: ;
;
②乙烯的电子式为: ,将电子式中的共用电子对换成短线即为结构式,乙烯的结构式为:
,将电子式中的共用电子对换成短线即为结构式,乙烯的结构式为: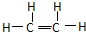 ,
,
故答案为: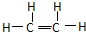 ;
;
(3)质量数为23,中子数为12的原子Na,其质子数为11和电子数为11,原子结构示意图: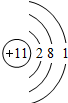 ,
,
故答案为: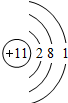 .
.
 ,故答案为:
,故答案为: ;
;②氨气分子中存在3个氮氢键,氮原子最外层达到8个电子稳定结构,氨气的电子式为
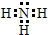 ,故答案为:
,故答案为: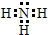 ;
;③NaOH中钠离子与氢氧根离子之间通过离子键结合,氧原子与氢原子之间存在H-O键,电子式为
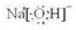 ,故答案为:
,故答案为: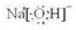 ;
;(2)①甲烷是碳原子和氢原子间通过共价单键形成的空间正四面体结构,结构式为:
 ,
,故答案为:
 ;
;②乙烯的电子式为:
 ,将电子式中的共用电子对换成短线即为结构式,乙烯的结构式为:
,将电子式中的共用电子对换成短线即为结构式,乙烯的结构式为: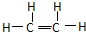 ,
,故答案为:
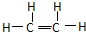 ;
;(3)质量数为23,中子数为12的原子Na,其质子数为11和电子数为11,原子结构示意图:
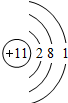 ,
,故答案为:
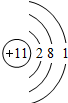 .
.
点评:本题考查了电子式、结构式、原子结构示意图的书写,题目难度中等,注意掌握电子式、结构式、原子结构示意图的概念及正确的表示方法,明确结构式、分子式、电子式、结构简式之间的区别.

练习册系列答案
相关题目
常温下,下列各组离子能大量共存的是( )
| A、无色溶液中:K+、CH3COO-、HCO3-、MnO4- |
| B、滴加石蕊呈红色的溶液:K+、NH4+、Cl-、S2- |
| C、pH=2的溶液中:NH4+、Na+、Cl-、Cu2+ |
| D、漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+ |
 德国化学家凯库勒认为苯分子的结构中,碳碳间以单、双键交替结合而成环状.为了评价凯库勒的观点,某学生设计了以下实验方案:
德国化学家凯库勒认为苯分子的结构中,碳碳间以单、双键交替结合而成环状.为了评价凯库勒的观点,某学生设计了以下实验方案:
