题目内容
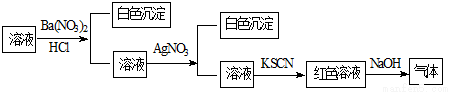
(11分)新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为 、 。
(2)闭合K开关后,a、b电极上均有气体产生.其中b电极上电极反应式为 ;
(3)若每个电池甲烷通入量为 1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积
为 L (标准状况)。
(1)2O2+4H2O+8e—= 8OH-;(3分),CH4+10OH--8e—= CO32 -+7H2O(3分)。
(2)2H2O + 2 e— = H2↑+ 2OH -(3分) 。
(3)4 (2分)。
【解析】
试题分析:(1)在甲烷燃料电池中通入甲烷的电极是负极,通入氧气的电极是正极,由于电解质溶液是KOH溶液,所以正极、负极的电极反应分别为2O2+4H2O+8e—= 8OH-; CH4+10OH--8e—= CO32 -+7H2O;(2)闭合K开关后,电极a与电源的正极连接,是阳极,b电极与电源的负极连接,是阴极。阴极b电极上发生还原反应,电极反应式为2H2O + 2 e— = H2↑+ 2OH -;(3)若每个电池甲烷通入量为 1 L(标准状况),且反应完全,由于在整个闭合回路中电子转移数目是(1L÷22.4L/mol)×8=(VL÷22.4L/mol)×2,解得V=4L。
考点:考查原电池、电解池的反应原理及应用的知识。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案(共12分)在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800 ℃,反应达到平衡时,NO的物质的量浓度是________;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
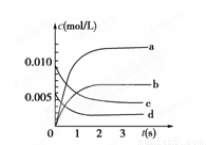
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂

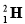 ②H2O、D2O ③
②H2O、D2O ③
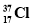 ④金刚石、石墨 ⑤O2、O3 ⑥H2、H+
④金刚石、石墨 ⑤O2、O3 ⑥H2、H+