题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、1.8g重水(D2O)中含NA个中子 |
| B、标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C、室温下,14g乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| D、足量的铜与含2molH2SO4的浓硫酸充分反应,可生成NA个SO2分子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量结合分子式和质子数+中子数=质量数计算;
B、依据n=
计算物质的量,结合氯气和碱反应自身氧化还原反应计算电子转移;
C、乙烯和丁烯最简式相同为CH2,依据n=
计算CH2物质的量得到碳原子数目;
D、浓硫酸和足量铜反应随反应进行浓度变稀后不能再和铜发生反应.
| m |
| M |
B、依据n=
| V |
| Vm |
C、乙烯和丁烯最简式相同为CH2,依据n=
| m |
| M |
D、浓硫酸和足量铜反应随反应进行浓度变稀后不能再和铜发生反应.
解答:
解:A、依据n=
计算物质的量=
=0.09mol,结合分子式和质子数+中子数=质量数计算,中子数=0.1mol×[4+16-(2+8)]×NA=NA个中子,故A正确;
B、依据n=
计算物质的量=
=0.1mol,结合氯气和碱反应自身氧化还原反应计算电子转移0.1NA,故B错误;
C、乙烯和丁烯最简式相同为CH2,依据n=
计算CH2物质的量=
=1mol,得到碳原子数目为NA,故C正确;
D、浓硫酸和足量铜反应随反应进行浓度变稀后不能再和铜发生反应,足量的铜与含2molH2SO4的浓硫酸充分反应,可生成SO2分子小于NA个,故D错误;
故选AC.
| m |
| M |
| 1.8g |
| 20g/mol |
B、依据n=
| V |
| Vm |
| 2.24L |
| 22.4L/mol |
C、乙烯和丁烯最简式相同为CH2,依据n=
| m |
| M |
| 14g |
| 14g/mol |
D、浓硫酸和足量铜反应随反应进行浓度变稀后不能再和铜发生反应,足量的铜与含2molH2SO4的浓硫酸充分反应,可生成SO2分子小于NA个,故D错误;
故选AC.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是微粒结构分析,注意浓硫酸变稀后不与铜发生反应,题目较简单.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
根据电子排布的特点,29Cu在周期表中属于( )
| A、s区 | B、p区 |
| C、d 区 | D、ds区 |
下列有关化学用语表示正确的是( )
| A、HClO的结构式:H-Cl-O |
B、Cl-的结构示意图: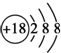 |
C、Na2O2的电子式: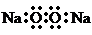 |
| D、Na原子外围电子排布式:3s1 |
下列有关化学用语正确的是( )
①乙烯的最简式C2H4
②乙醛的结构简式CH3COH
③四氯化碳的电子式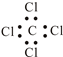
④乙烷的结构式CH3CH3.
①乙烯的最简式C2H4
②乙醛的结构简式CH3COH
③四氯化碳的电子式

④乙烷的结构式CH3CH3.
| A、全对 | B、全错 | C、①② | D、③④ |
下列事实不能证明氨水是弱碱的是( )
| A、pH=11的氨水加入水稀释到原溶液体积100倍时,pH大于9 |
| B、氯化铵溶液呈酸性 |
| C、常温下0.01 mol/L氨水的pH=10.6 |
| D、体积相同的0.1 mol/L氨水和0.1 mol/L NaOH溶液中和盐酸的量相同 |
等浓度的下列稀溶液:①乙酸、②硫酸氢钠、③碳酸、④乙醇,它们的pH由小到大排列顺序正确的是( )
| A、④②③① | B、③①②④ |
| C、②①③④ | D、①②③④ |
国际上不提倡伊朗浓缩铀,因为铀-235(
U)是制造原子弹的燃料.
U原子核内含有中子数为( )
235 92 |
235 92 |
| A、92 | B、235 |
| C、143 | D、327 |
