题目内容
5.(1)下列物质的分子与O3分子的结构最相似的是C.A.H2O B.CO2 C.SO2 D.BeCl2
(2)O3分子是否为极性分子?是(填“是”或“否”)
分析 (1)根据分子中中心原子的价层电子对数判断分子的空间构型;
(2)分子中正负电荷中心不重合,这样的分子为极性分子;分子中正负电荷的重心重合,则为非极性分子.
解答 解:(1)O3分子的结构如图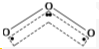 ,在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子呈V形,
,在臭氧O3中,中心的氧原子以sp2杂化,与两旁的配位氧原子键合生成两个σ键,使O3分子呈V形,
A.H2O中含有2对σ键,2对孤电子对,O原子sp3杂化,空间结构为V形,故A错误;
B.CO2为含有4个σ键,没有孤电子对,为sp杂化,空间结构为直线形,故B错误;
C.SO2分子呈“V”字形结构,其成键方式与O3类似,S原子sp2杂化,S原子和两侧的氧原子除以σ键结合以外,还形成一个三中心四电子的大π键,故C正确;
D.BeCl2含有2个σ键,没有孤电子对,为sp杂化,空间结构为直线形,故D错误;
故答案为:C;
(2)O3中的中心O原子为sp2杂化,理想模型为平面三角形,分子构型为V型,而且O3形成的是三中心四电子大π键,空间构型不对称.正负电荷重心不重合,所以是极性分子,
故答案为:是.
点评 本题考查了物质结构,涉及杂化轨道理论、空间构型的判断等知识点,题目难度中等,旨在考查学生灵活运用基础知识解决实际问题的能力,注意杂化理论的熟练应用方法.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
17.某混合烃有甲烷和乙烯组成,将2L该混合烃燃烧后得2.8L CO2和4L水蒸汽,则该混合烃中,甲烷和乙烯的体积比为( )
| A. | 2:3 | B. | 3:2 | C. | 1:4 | D. | 4:1 |
15.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、电子天平、药匙、量筒、玻璃棒、500 mL容量瓶、胶头滴管.(在横线上填写所缺仪器的名称)
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
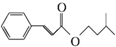 )是一种香料,一种合成路线如图:
)是一种香料,一种合成路线如图: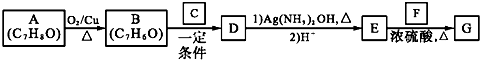
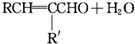
 +CH3CHO$\stackrel{一定条件}{→}$
+CH3CHO$\stackrel{一定条件}{→}$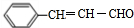 +H2O.
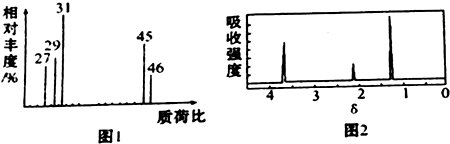
+H2O.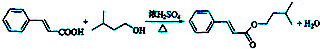 .
.
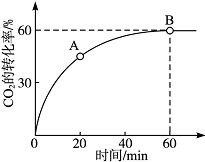 尿素[CO(NH2)2]是首个由无机物人工合成的有机物
尿素[CO(NH2)2]是首个由无机物人工合成的有机物