题目内容
8.反应将4molSO2,2molO2放入4L密闭容器中进行反应.2min后达到平衡时SO3的浓度为0.5mol/L.用O2的浓度变化表示2min内的化学反应速率为0.25mol/(L•min),此条件下的平衡常数k为4.分析 利用化学平衡三段式计算各组分的浓度,根据v=$\frac{△c}{△t}$计算出用O2的浓度变化表示2min内的化学反应速率,根据平衡常数公式K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})•c({O}_{2})}$计算出该反应的平衡常数.
解答 解:平衡时SO3的浓度为0.5mol•L-1,则:
2SO2(g)+O2(g)?2SO3(g),
起始量(mol•L-1) 1 0.5 0
变化量(mol•L-1) 0.5 0.25 0.5
平衡量(mol•L-1) 0.5 0.25 0.5
用O2的浓度变化表示2min内的化学反应速率为:v(O2)=$\frac{0.25mol/L}{2min}$=0.25mol/(L•min);
该反应的平衡常数K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})•c({O}_{2})}$=$\frac{0.{5}^{2}}{0.{5}^{2}×0.25}$=4,
故答案为:0.25mol/(L•min);
点评 本题考查了化学平衡的计算,题目难度不大,明确化学平衡常数、化学反应速率的概念及表达式为解答关键,注意掌握三段式在化学平衡计算中的应用,试题培养了学生的化学计算能力.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
8.能正确表示下列反应的离子方程式的是( )
| A. | 将铁粉加入稀硫酸中:Fe+2H+═Fe2++H2↑ | |
| B. | NaHCO3溶液中加入HCl:CO32-+2H+═CO2↑+H2O | |
| C. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl═Mn2++2Cl-+Cl2↑+2H2O |
13.某同学用工业硫酸铜(含硫酸亚铁等杂质)制备纯净的CuSO4•5H2O.工艺流程如下(部分操作和条件略):
I.取工业硫酸铜固体,用稀硫酸溶解,过滤.
II.向滤液中滴加H2O2溶液,稍加热.
III.向II的溶液中加入CuO粉末至pH=4.
IV.加热煮沸,过滤,滤液用稀硫酸酸化至pH=1.
V.蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得晶体.
已知部分阳离子生成氢氧化物的pH、Ksp(25℃)如下表:
(1)II中发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)II中将Fe2+氧化为Fe3+的目的是在调节在pH=4时,只将Fe3+转化为沉淀除去,而不会使Cu2+转化为沉淀.
(3)用K3[Fe(CN)6](铁氰化钾)验证II中Fe2+是否转化完全的现象是若有蓝色沉淀生说,说明Fe2+没有完全转化;若没有蓝色沉淀生成,说明Fe2+已经完全转化.
(4)III中发生反应的离子方程式是2Fe3++3CuO+3H2O=2Fe(OH)3+3Cu2+.
通过计算说明在此条件下的溶液中Fe3+是否沉淀完全(提示:当溶液中某离子浓度小于1.0×10-5 mol•L-1时可认为该离子沉淀完全).
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因用稀硫酸酸化至PH=1,可以抑制Cu2+在加热过程中水解,以获得纯净的硫酸铜晶体
(6)V中获得晶体的方法是蒸发浓缩、冷却结晶.
I.取工业硫酸铜固体,用稀硫酸溶解,过滤.
II.向滤液中滴加H2O2溶液,稍加热.
III.向II的溶液中加入CuO粉末至pH=4.
IV.加热煮沸,过滤,滤液用稀硫酸酸化至pH=1.
V.蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得晶体.
已知部分阳离子生成氢氧化物的pH、Ksp(25℃)如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| 开始沉淀时pH | 2.7 | 7.6 | 4.7 |
| 完全沉淀时pH | 3.7 | 9.6 | 6.7 |
| Ksp | 4.0×10-38 | 8.0×10-16 | 2.2×10-20 |
(2)II中将Fe2+氧化为Fe3+的目的是在调节在pH=4时,只将Fe3+转化为沉淀除去,而不会使Cu2+转化为沉淀.
(3)用K3[Fe(CN)6](铁氰化钾)验证II中Fe2+是否转化完全的现象是若有蓝色沉淀生说,说明Fe2+没有完全转化;若没有蓝色沉淀生成,说明Fe2+已经完全转化.
(4)III中发生反应的离子方程式是2Fe3++3CuO+3H2O=2Fe(OH)3+3Cu2+.
通过计算说明在此条件下的溶液中Fe3+是否沉淀完全(提示:当溶液中某离子浓度小于1.0×10-5 mol•L-1时可认为该离子沉淀完全).
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因用稀硫酸酸化至PH=1,可以抑制Cu2+在加热过程中水解,以获得纯净的硫酸铜晶体
(6)V中获得晶体的方法是蒸发浓缩、冷却结晶.
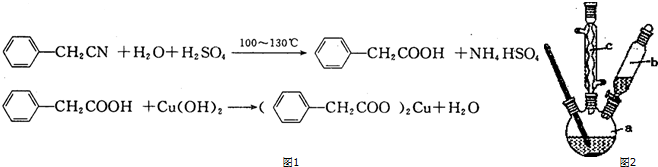
18.某实验小组利用如图装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式.
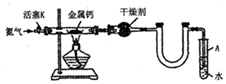
(1)按图连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热.冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好.
(2)反应过程中末端导管必须始终插入试管A的水中,目的是防止反应过程中空气进入反应管.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应; ③反应结束后,防止反应过程中空气进入反应管;④拆除装置,取出产物.
(4)上述步骤①中通入N2-段时间后再点燃酒精灯原因是氮气排尽装置中的空气,可以防止钙与装置中的氧气或二氧化碳、水等反应,装置中干燥管后的U形管的作用是防倒吸.
(5)数据记录如表:
①计算得到实验式CaxN2,其中x=$\frac{14}{5}$.
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:O2和N2分别与等量的Ca反应,生成CaO的质量高于Ca3N2.若通入的N2中混有少量的O2,会导致计算出n(N)偏大,所以 $\frac{n(Ca)}{n(N)}$<$\frac{3}{2}$,即x<3.

(1)按图连接好实验装置,检查装置的气密性,方法是关闭活塞K,微热反应管,试管A中有气泡冒出,停止加热.冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好.
(2)反应过程中末端导管必须始终插入试管A的水中,目的是防止反应过程中空气进入反应管.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应; ③反应结束后,防止反应过程中空气进入反应管;④拆除装置,取出产物.
(4)上述步骤①中通入N2-段时间后再点燃酒精灯原因是氮气排尽装置中的空气,可以防止钙与装置中的氧气或二氧化碳、水等反应,装置中干燥管后的U形管的作用是防倒吸.
(5)数据记录如表:
| 空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
| 14.80 | 15.08 | 15.15 |
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:O2和N2分别与等量的Ca反应,生成CaO的质量高于Ca3N2.若通入的N2中混有少量的O2,会导致计算出n(N)偏大,所以 $\frac{n(Ca)}{n(N)}$<$\frac{3}{2}$,即x<3.
 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O.
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.该电池反应的化学方程式为2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O.
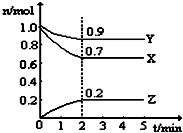 某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: