题目内容
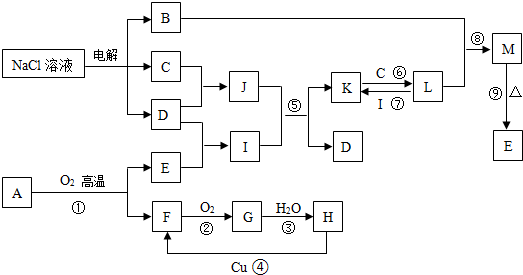
下列框图中,各物质均为中学化学常见物质.已知反应①②③是工业上制取H的三个反应,M是红褐色物质,且难溶于水.
试回答下列问题:
(1)M的化学式是 ;D的化学式是 .
(2)检验L中金属阳离子的常用方法是 .
(3)反应⑦的化学方程式是 .
(4)反应④的化学方程式是 .在此反应中,如果有6.4gCu参加反应,则被还原的H的质量是 g.

试回答下列问题:
(1)M的化学式是
(2)检验L中金属阳离子的常用方法是
(3)反应⑦的化学方程式是
(4)反应④的化学方程式是
分析:电解食盐水,可生成H2、Cl2和NaOH,M为红褐色物质,且难溶于水,应为Fe(OH)3,且与B和L生成,则B应为NaOH,则C、D应为H2、Cl2,可知J为HCl,K为FeCl2,L为FeCl3,结合转化关系可知C为Cl2,D为H2,Fe(OH)3分解生成的E为Fe2O3,反应①②③是工业上制取H的三个反应,且生成的E为Fe2O3,可知A中含有Fe元素,应为工业生成硫酸的反应,由转化关系可知A为FeS2,F为SO2,G为SO3,H为H2SO4,结合对应物质的性质以及题目要求解答该题.
解答:解:电解食盐水,可生成H2、Cl2和NaOH,M为红褐色物质,且难溶于水,应为Fe(OH)3,且与B和L生成,则B应为NaOH,则C、D应为H2、Cl2,可知J为HCl,K为FeCl2,L为FeCl3,结合转化关系可知C为Cl2,D为H2,Fe(OH)3分解生成的E为Fe2O3,反应①②③是工业上制取H的三个反应,且生成的E为Fe2O3,可知A中含有Fe元素,应为工业生成硫酸的反应,由转化关系可知A为FeS2,F为SO2,G为SO3,H为H2SO4,
(1)由以上分析可知M为Fe(OH)3,D为H2,故答案为:Fe(OH)3;H2;
(2)L为FeCl3,可与KSCN发生反应,溶液变为血红色,检验方法为取少量L溶液,滴加KSCN溶液,若溶液变为血红色,说明含有Fe3+(或取少量L溶液,滴加NaOH溶液,若生成红褐色沉淀,说明含有Fe3+),
故答案为:取少量L溶液,滴加KSCN溶液,若溶液变为血红色,说明含有Fe3+(或取少量L溶液,滴加NaOH溶液,若生成红褐色沉淀,说明含有Fe3+);
(3)L为FeCl3,可与铁反应生成FeCl2,反应的方程式为2FeCl3+Fe=3FeCl2,故答案为:2FeCl3+Fe=3FeCl2;
(4)浓硫酸具有强氧化性,可在加热条件下与铜发生氧化还原反应,反应的方程式为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,
由方程式可知,如果有6.4gCu参加反应,即0.1mol铜被氧化,则参加反应的硫酸为0.2mol,其中被还原的物质的量为0.1mol,质量为9.8g,
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;9.8g.
(1)由以上分析可知M为Fe(OH)3,D为H2,故答案为:Fe(OH)3;H2;
(2)L为FeCl3,可与KSCN发生反应,溶液变为血红色,检验方法为取少量L溶液,滴加KSCN溶液,若溶液变为血红色,说明含有Fe3+(或取少量L溶液,滴加NaOH溶液,若生成红褐色沉淀,说明含有Fe3+),
故答案为:取少量L溶液,滴加KSCN溶液,若溶液变为血红色,说明含有Fe3+(或取少量L溶液,滴加NaOH溶液,若生成红褐色沉淀,说明含有Fe3+);
(3)L为FeCl3,可与铁反应生成FeCl2,反应的方程式为2FeCl3+Fe=3FeCl2,故答案为:2FeCl3+Fe=3FeCl2;
(4)浓硫酸具有强氧化性,可在加热条件下与铜发生氧化还原反应,反应的方程式为Cu+2H2SO4(浓)
| ||
由方程式可知,如果有6.4gCu参加反应,即0.1mol铜被氧化,则参加反应的硫酸为0.2mol,其中被还原的物质的量为0.1mol,质量为9.8g,
故答案为:Cu+2H2SO4(浓)
| ||
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力的考查,本题的突破口为M为红褐色物质,本题信息量大,涉及物质的种类多,注意把握物质的转化关系,牢固把握相关基础知识为解答该类题目的关键,难度中等.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
(12分)下列框图中,各物质均为中学化学常见物质。已知反应①②③是工业上制取H的三个反应,M是红褐色物质,且难溶于水。
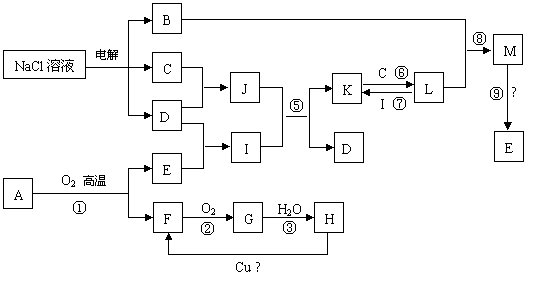 |
试回答下列问题:
⑴M的化学式是 ;D的化学式是 。
⑵检验L中金属阳离子的常用方法是 。
⑶反应⑦的化学方程式是 。
⑷反应④的化学方程式是 。在此反应中,如果有6.4gCu参加反应,则被还原的H的质量是 g。
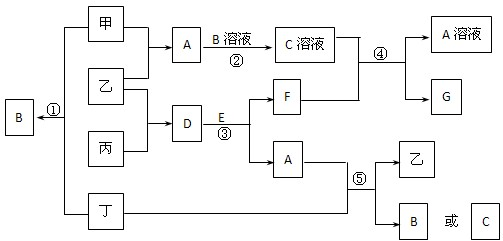
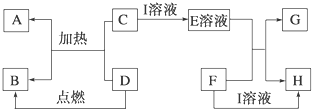 在如图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质.C为一种黑色粉末,D为一种气体.请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
在如图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质.C为一种黑色粉末,D为一种气体.请根据框图中物质的转化关系及相关信息,用化学式填写下列空白: