题目内容
下列有机物中含有少量杂质(括号中是杂质),除杂方法正确的是( )
| A、乙醇(乙酸):加入碳酸钠溶液,振荡,静置,分液 |
| B、硝基苯(硫酸):将其加入NaOH溶液中,振荡,静置,分液 |
| C、乙醛(乙酸乙酯):加入氢氧化钠溶液,振荡,静置,分液 |
| D、溴乙烷(溴):加入四氯化碳,振荡,静置,分液 |
考点:物质的分离、提纯的基本方法选择与应用
专题:化学实验基本操作
分析:A.乙醇易溶于水,乙酸生成溶于水的乙酸钠;
B.硝基苯不溶于氢氧化钠溶液,硫酸与氢氧化钠发生中和反应;
C.乙醛溶于水,乙酸乙酯溶于氢氧化钠溶液;
D.溴乙烷、溴都溶于四氯化碳.
B.硝基苯不溶于氢氧化钠溶液,硫酸与氢氧化钠发生中和反应;
C.乙醛溶于水,乙酸乙酯溶于氢氧化钠溶液;
D.溴乙烷、溴都溶于四氯化碳.
解答:
解:A.乙醇易溶于水,乙酸生成溶于水的乙酸钠,应用蒸馏的方法分离,故A错误;
B.硝基苯不溶于氢氧化钠溶液,硫酸与氢氧化钠发生中和反应,可用分液的方法分离,故B正确;
C.乙醛溶于水,乙酸乙酯溶于氢氧化钠溶液,应用蒸馏的方法分离,故C错误;
D.溴乙烷、溴都溶于四氯化碳,应用氢氧化钠溶液分离,故D错误.
故选B.
B.硝基苯不溶于氢氧化钠溶液,硫酸与氢氧化钠发生中和反应,可用分液的方法分离,故B正确;
C.乙醛溶于水,乙酸乙酯溶于氢氧化钠溶液,应用蒸馏的方法分离,故C错误;
D.溴乙烷、溴都溶于四氯化碳,应用氢氧化钠溶液分离,故D错误.
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、实验基本操作及离子检验等,把握物质的性质及实验原理为解答的关键,注意实验操作的可行性、实验方案的可行性分析,题目难度不大.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、向氯化铁溶液中加入铁:Fe3++Fe=2Fe2+ |
| B、向AlCl3溶液中加入足量的氨水:Al3++4OH-=AlO2-+2H2O |
| C、铜与稀硝酸的反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
| D、氯气和水的反应:Cl2+H2O=2H++Cl-+ClO- |
用下列装置进行对应的实验(部分仪器已省略),能达到实验目的是( )
A、 吸收HCl |
B、 干燥Cl2 |
C、 石油的蒸馏 |
D、 吸收NH3 |
根据下列框图,有关说法正确的是( )


| A、M、E都是第四周期中的过渡元素,E的金属活动性比M的金属活动性强,E3+的氧化性比M2+的氧化性弱 |
| B、反应⑤的离子方程式可表示为:2E(OH)3+3Cl2+6H2O═3EO42-+6Cl-+12H+ |
| C、用K2EO4、Zn可制成一种高能电池,该电池中负极的电极反应式为:EO42-+4H2O+3e-═E(OH)3+5OH- |
| D、反应①、②、③、⑤都属于氧化还原反应,且在反应①和③中硫酸仅表现了酸性 |
下列实验操作或装置(略去部分加持仪器)正确的是( )
A、 配制溶液 |
B、 分离互不相容的两种液体 |
C、 吸收HCl |
D、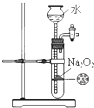 制备少量氧气 |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是( )
A、 |
B、 |
C、 |
D、 |
 用测量压强的仪器测定生铁在90%醋酸溶液中发生腐蚀的装置及容器内压强随时间变化如图所示,下列分析错误的是( )
用测量压强的仪器测定生铁在90%醋酸溶液中发生腐蚀的装置及容器内压强随时间变化如图所示,下列分析错误的是( )| A、0~t1,可能发生了析氢腐蚀压强增大 |
| B、0~t1,可能反应放热温度升高压强增大 |
| C、t2时压强小于起始压强,一定发生了吸氧腐蚀 |
| D、整个过程中铁粉发生了还原反应生成Fe2+ |
