题目内容
能在水溶液中大量共存的一组离子是
A.H+、I―、NO3―、SiO32-
B.Ag+、Fe3+、Cl―、SO42―
C.K+、SO42-、Cu2+、NO3―
D.NH4+、OH-、Cl-、HCO3-
C
【解析】
试题分析:A.酸性条件下NO3―具有很强的氧化性,能氧化I―,B. Ag+和Cl―反应生成难溶物氯化银;C.根离子能大量共存;D.NH4+与OH-、OH-与HCO3-反应生成弱电解质;选C。
考点:考查离子共存。

练习册系列答案
相关题目
下列对一些实验事实的理论解释正确的是
| 实验事实 | 理论解释 |
A | SO2溶于水形成的溶液能导电 | SO2是电解质 |
B | 白磷为正四面体分子 | 白磷分子中P—P间的键角是109°28′ |
C | 1体积水可以溶解700体积氨气 | 氨是极性分子;可与水形成氢键;且与水反应 |
D | HF的沸点高于HCl | H—F的键长比H—Cl的键长短 |
某学生用NaHCO3和KHCO3组成的某固体混合物进行实验,测得如下表数据(盐酸的物质的量浓度相等):
实验编号 | ① | ② | ③ |
盐酸体积 | 50mL盐酸 | 50mL盐酸 | 50mL盐酸 |
m(混合物) | 9.2g | 16.56g | 27.6g |
V(CO2)(标准状况) | 2.24L | 3.36L | 3.36L |
分析表中数据,下列说法不正确的是( )
A.由①可以计算出盐酸的物质的量浓度
B.由②、③可知:混合物质量增加,气体体积没有变化,说明盐酸已经反应完全
C.由①、②可知:①中的固体不足而完全反应
D.由①可以计算出混合物的NaHCO3的质量分数
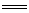 2ZnO(s)△H=-701.0kJ·mol-1
2ZnO(s)△H=-701.0kJ·mol-1