题目内容
6.碱式碳酸铜可表示为:xCuCO3•yCu(OH)2•zH2O.测定碱式碳酸铜组成的方法有多种.现采用氢气还原法测定,其化学反应方程为:xCuCO3•yCu(OH)2•zH2O+(x+y)H2=(x+y)Cu+xCO2+(x+2y+z)H2O请回答如下问题:
(1)实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→kj→gf→(d)(e)→hi→bc→(l)
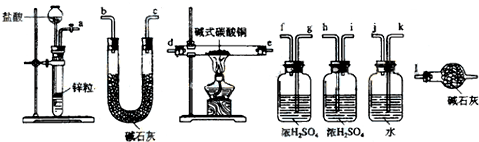
(2)用于装盐酸的仪器名称为长颈漏斗;
(3)实验中浓硫酸的作用分别为吸收氢气中的水蒸气、吸收氢气还原碱式碳酸铜反应生成的水蒸气;
(4)称取24.0g某碱式碳酸铜样品,充分反应后得到12.8g残留物,生成4.4g二氧化碳和7.2g水.化学式为CuCO3•Cu(OH)2•H2O;
(5)若没有装置l会有什么影响碱石灰吸收空气中的水蒸气和二氧化碳质量增大,导致测定还原生成的二氧化碳质量增大.
分析 采用氢气还原法测定,利用装置制备氢气,用干燥的氢气与碱式碳酸铜反应,通过测定生成的二氧化碳和水以及反应后固体的质量来确定物质的组成,为防止空气中CO2和H2O进入U型干燥装置,可在最后再连接一个盛有碱石灰的干燥装置来吸收空气中的二氧化碳和水;
(1)本实验的原理,用干燥的氢气与碱式碳酸铜反应,通过测定生成的二氧化碳和水以及反应后固体的质量来确定物质的组成,为防止空气中CO2和H2O进入U型干燥装置,可在最后再连接一个盛有碱石灰的干燥装置来吸收空气中的二氧化碳和水;
(2)装置图中仪器形状和用途可知用于装盐酸的仪器名称为长颈漏斗;
(3)浓硫酸在通入硬质玻璃管前是干燥氢气,在玻璃管后是吸收生成水蒸气,测定水的质量;
(4)根据化学方程式生成物之间的质量关系求出x、y、z,根据生成的水和反应物中水的关系求解水的质量;
(5)若没有装置l,还原产物通过浓硫酸后通过碱石灰,会吸收空气中二氧化碳和水蒸气测定二氧化碳质量增大;
解答 解:(1)本实验的原理,用干燥的氢气融入与碱式碳酸铜反应,通过测定生成的二氧化碳和水以及反应后固体的质量来确定物质的组成,为防止空气中CO2和H2O进入U型干燥装置,可在最后再连接一个盛有碱石灰的干燥装置来吸收空气中的二氧化碳和水;氢气流方向的连接顺序是a→kj→gf→de→hi→bc→l,
故答案为:kj→gf→de→hi→bc;
(2)装置图中仪器形状和用途可知用于装盐酸的仪器名称为长颈漏斗,故答案为:长颈漏斗;
(3)浓硫酸在通入硬质玻璃管前是干燥氢气,在玻璃管后是吸收生成水蒸气,测定水的质量,
故答案为:吸收氢气中的水蒸气;吸收氢气还原碱式碳酸铜反应生成的水蒸气;
(4)xCuCO3•yCu(OH)2•zH2O+( x+y)H2=(x+y)Cu+xCO2↑+(x+2y+z)H2O
64(x+y) 44x 18(x+2y+z)
12.7g 4.4g 7.2g
$\frac{64(x+y)}{12.7g}$=$\frac{44x}{4.4g}$$\frac{44x}{4.4g}$=$\frac{18(x+2y+z)}{7.2g}$
解得:y=x
$\frac{44x}{4.4g}$=$\frac{18(x+2y+z)}{7.2g}$
解得:z=x
令x=1,则y=1,z=1,则化学式为CuCO3•Cu(OH)2•H2O,
故答案为:CuCO3•Cu(OH)2•H2O;
(5)若没有装置l,会影响测定生成二氧化碳的质量,还原产物通过浓硫酸后通过碱石灰,会吸收空气中二氧化碳和水蒸气,使测定二氧化碳质量增大,
故答案为:碱石灰吸收空气中的水蒸气和二氧化碳质量增大,导致测定还原生成的二氧化碳质量增大;
点评 本题考查了物质组成的实验探究,主要是实验原理的分析判断、实验过程、实验中测定产物的实验方法及其化学方程式计算,提炼题干信息,掌握实验基本操作是解题关键,题目难度中等.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 纯碱溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| B. | 醋酸溶液显酸性:CH3COOH+H2O?CH3COO-+H3O+ | |
| C. | 向碘化亚铁溶液中通入足量的溴水:3Br2+2Fe2++4I-═6Br-+2Fe3++2I2 | |
| D. | 向碳酸氢钙溶液中滴加过量的烧碱溶液:HCO3-+Ca2++2OH-═CaCO3↓+H2O |
| A. | 电解水生成氢气和氧气时,电能转化为化学能 | |
| B. | 煤燃烧时,化学能主要转化为热能 | |
| C. | 绿色植物进行光合作用时,太阳能转化为化学能 | |
| D. | 白炽灯工作时,化学能主要转化为光能 |


 如图所示为相互串联的甲、乙两电解池.试回答:
如图所示为相互串联的甲、乙两电解池.试回答: