题目内容
下列有关化学用语正确的是( )
A、O原子的电子排布图为 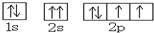 |
| B、氯化钠的分子式:NaCl |
C、Cl-的结构示意图: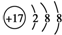 |
| D、Ca原子的电子排布式为 1s22s22p63s23p63d2 |
考点:原子核外电子排布,原子结构示意图,分子式
专题:
分析:A、2s电子自旋方向应该相反,能够最低进行判断;
B、氯化钠没有分子式;
C、根据构造原理判断氯离子的结构示意图;
D、根据构造原理判断钙原子的电子排布式.
B、氯化钠没有分子式;
C、根据构造原理判断氯离子的结构示意图;
D、根据构造原理判断钙原子的电子排布式.
解答:
解:A、原子的电子排布图中,该元素2s的两个电子的自旋方向应该相反,正确为: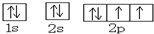 ,必须满足能量最低,故A错误;
,必须满足能量最低,故A错误;
B、氯化钠没有分子式、只有化学式,故B错误;
C、根据构造原理,Cl-的结构示意图: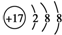 ,故C正确;
,故C正确;
D、根据构造原理,Ca原子的电子排布式为 1s22s22p63s23p64s2,故D错误;
故选C.
 ,必须满足能量最低,故A错误;
,必须满足能量最低,故A错误;B、氯化钠没有分子式、只有化学式,故B错误;
C、根据构造原理,Cl-的结构示意图:
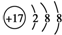 ,故C正确;
,故C正确;D、根据构造原理,Ca原子的电子排布式为 1s22s22p63s23p64s2,故D错误;
故选C.
点评:本题考查了电子式、原子结构示意图等化学用语的表示方法,可以所学知识进行判断,本题难度不大.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
下列溶液中各微粒的浓度关系正确的是( )
| A、1 L 0.1 mol?L-1CuSO4?(NH4)2SO4?6H2O的溶液中:c(NH4+)>c(SO42-)>c(Cu2+)>c(H+)>c(OH-) |
| B、0.2 mol?L-1NH4NO3和0.l mol?L-1 NaOH溶液等体积混合后:c(NO3-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) |
| C、0.1 mol?L-1 NaHCO3溶液中:c(Na+)+c(H+)<c(HCO3-)+c(CO32-)+c(H2CO3)+c(OH-) |
| D、等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
常温下的下列溶液,有关说法正确的是( )
| A、某酸H2A的钠盐NaHA溶液中:c(A2-)<c(H2A),则该溶液的pH>7 |
| B、1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-8mol/L盐酸的pH=8.0 |
| C、在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| D、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
在氧化还原反应CuO+H2
Cu+H2O中,还原产物是( )
| ||
| A、CuO |
| B、H2 |
| C、Cu |
| D、H2O |
反应①是自海藻灰中提取碘的主要反应,反应②是自智利硝石中提取碘的主要反应:①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2;②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2.已知NaIO3的氧化性与MnO2相近,下列有关说法正确的是( )
| A、两个反应中生成等量的I2时转移的电子数相等 |
| B、I2在反应①②中都是氧化产物 |
| C、NaI和NaIO3在一定条件下能反应生成I2 |
| D、NaIO3在任何化学反应中只能作氧化剂,不能作还原剂 |
在体积相同的三个容器里分别充入三种气体①氢气;②二氧化碳;③氧气,并保持三个容器内气体的温度和密度均相等,下列说法正确的是( )
| A、分子数目:①=②=③ |
| B、质量关系:①<③<② |
| C、压强关系:①>③>② |
| D、原子数目:②>③>① |
下列离子方程式正确的是( )
| A、磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | ||||
| B、NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | ||||
C、用石墨电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| D、铅蓄电池放电时的负极反应:PbSO4+2H2O-2e-═PbO2+4H++SO42- |