题目内容
如图是实验室制备1,2一二溴乙烷并进行一系列相关实验的装置(加热及夹持设备已略).
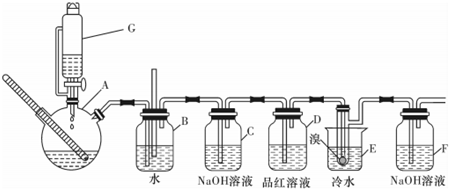
有关数据列表如下:
请按要求回答下列问题:
(1)装置G的名称为 ,G中药品为1,3的无水乙醇和浓硫酸混合液,写出制备乙烯的化学反应方程式:
(2)装置B中长直导管的作用是
(3)反应过程中应用冷水冷却装置E中大试管,但又不能过度冷却(如用冰水),其原因是
(4)某学生发现反应结束时,G中试剂消耗量大大超过理论值(装置不漏气),其原因是
(5)有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,其原因是
(6)若消耗无水乙醇的体积为100mL,制得1,2一二溴乙烷的体积为40mL,则该反应的产率为 .

有关数据列表如下:
| 乙醇 | 1.2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/(g/cm) | 0.79 | 2.2 | 0.71 |
| 沸点/ | 78.5 | 132 | 34.6 |
| 熔点/ | -130 | 9 | -116 |
(1)装置G的名称为
(2)装置B中长直导管的作用是
(3)反应过程中应用冷水冷却装置E中大试管,但又不能过度冷却(如用冰水),其原因是
(4)某学生发现反应结束时,G中试剂消耗量大大超过理论值(装置不漏气),其原因是
(5)有学生提出,装置F中可改用足量的四氯化碳液体吸收多余的气体,其原因是
(6)若消耗无水乙醇的体积为100mL,制得1,2一二溴乙烷的体积为40mL,则该反应的产率为
考点:溴乙烷的制取
专题:实验题,有机物的化学性质及推断
分析:(1)G的名称为连通滴液漏斗;乙醇在浓硫酸作催化剂加热170℃时生成乙烯;
(2)长直导管的作用是防止倒吸;
(3)液溴易挥发,冷水冷却,能减少液溴挥发,由表中数据可知温度太低,1,2-二溴乙烷会凝结为固体;
(4)乙醇在浓硫酸作催化剂作用下会有乙醚等副产物生成,反应太剧烈时乙醇部分挥发;
(5)根据尾气的成分是乙烯和溴分析;
(6)先求出n(乙醇)=(100mL×0.79g/ml)÷46g/mol=17.1739mol,n(溴乙烷)=(40mL×2.2g/ml)÷188g/mol=0.4681mol,然后根据转化率的概念来解答.
(2)长直导管的作用是防止倒吸;
(3)液溴易挥发,冷水冷却,能减少液溴挥发,由表中数据可知温度太低,1,2-二溴乙烷会凝结为固体;
(4)乙醇在浓硫酸作催化剂作用下会有乙醚等副产物生成,反应太剧烈时乙醇部分挥发;
(5)根据尾气的成分是乙烯和溴分析;
(6)先求出n(乙醇)=(100mL×0.79g/ml)÷46g/mol=17.1739mol,n(溴乙烷)=(40mL×2.2g/ml)÷188g/mol=0.4681mol,然后根据转化率的概念来解答.
解答:
解:(1)G的名称为连通滴液漏斗;乙醇在浓硫酸作催化剂加热170℃时生成乙烯,方程式为:其反应方程式为:CH3CH2OH
CH2=CH2↑+H2O,
故答案为:连通滴液漏斗;CH3CH2OH
CH2=CH2↑+H2O;
(2)长直导管的作用是防止倒吸,故答案为:防止倒吸;
(3)液溴易挥发,反应过程中应用冷水冷却装置E,能减少液溴挥发,由表中数据可知1,2-二溴乙烷的熔点为9℃,如用冰水冷却时温度太低,1,2-二溴乙烷会凝结为固体,从而导致导管堵塞;
故答案为:1,2-二溴乙烷易凝结成固体而发生堵塞;
(4)乙醇在浓硫酸作催化剂作用下会有乙醚等副产物生成,反应太剧烈时乙醇部分挥发;
故答案为:副反应发生或反应太剧烈乙醇部分挥发;
(5)实验中尾气的成分是乙烯和溴,二者都易溶于四氯化碳,所以能用四氯化碳液体吸收多余的气体;
故答案为:尾气的成分是乙烯和溴,二者都易溶于四氯化碳;
(6)n(乙醇)=(100mL×0.79g/ml)÷46g/mol=1.7173mol,n(1,2-二溴乙烷)=(40mL×2.2g/ml)÷188g/mol=0.4681mol,该反应的产率为
×100%=27.26%;
故答案为:27.26%.
| 浓硫酸 |
| 170℃ |
故答案为:连通滴液漏斗;CH3CH2OH
| 浓硫酸 |
| 170℃ |
(2)长直导管的作用是防止倒吸,故答案为:防止倒吸;
(3)液溴易挥发,反应过程中应用冷水冷却装置E,能减少液溴挥发,由表中数据可知1,2-二溴乙烷的熔点为9℃,如用冰水冷却时温度太低,1,2-二溴乙烷会凝结为固体,从而导致导管堵塞;
故答案为:1,2-二溴乙烷易凝结成固体而发生堵塞;
(4)乙醇在浓硫酸作催化剂作用下会有乙醚等副产物生成,反应太剧烈时乙醇部分挥发;
故答案为:副反应发生或反应太剧烈乙醇部分挥发;
(5)实验中尾气的成分是乙烯和溴,二者都易溶于四氯化碳,所以能用四氯化碳液体吸收多余的气体;
故答案为:尾气的成分是乙烯和溴,二者都易溶于四氯化碳;
(6)n(乙醇)=(100mL×0.79g/ml)÷46g/mol=1.7173mol,n(1,2-二溴乙烷)=(40mL×2.2g/ml)÷188g/mol=0.4681mol,该反应的产率为
| 0.4681mol |
| 1.7173mol |
故答案为:27.26%.
点评:本题主要考查了仪器的识别、化学实验的基本操作、物质的产率等知识,难度不大,注意反应原理的掌握.

练习册系列答案
相关题目
下列说法正确的是( )
| A、液态氯化氢、固态氯化钠不导电,所以HCl、NaCl不是电解质 |
| B、NH3、CO2水溶液均能导电,所以NH3、CO2均是电解质 |
| C、蔗糖、酒精在水溶液中或熔化时不导电,所以它们不是电解质 |
| D、铜、石墨均导电,所以它们是电解质 |
下面有关Na2CO3与NaHCO3的说法正确的是( )
| A、热稳定性:NaHCO3>Na2CO3 |
| B、相同浓度溶液的碱性:Na2CO3<NaHCO3 |
| C、都能与酸反应放出CO2,但剧烈程度:NaHCO3>Na2CO3 |
| D、Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 |
据报道用Mg与石墨作电极与NH4Cl溶液形成原电池(盐桥为装有琼胶的饱和KCl溶液),也可生成NH3.下列说法正确是( )
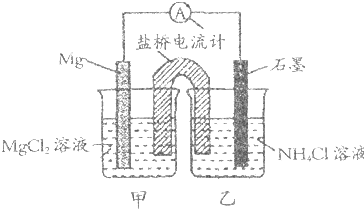

| A、石墨电极反应式为2NH4++2e-=2NH3↑+H2↑ |
| B、乙烧杯中一直存在:c(Cl-)<c(NH4+) |
| C、电子流向是由石墨→导线→Mg |
| D、盐桥中的Cl-移向乙烧杯 |
室温下,取O.2mol/L H2A溶液与xmol/L NaOH溶液等体积混合(忽略混合后溶液体积变化),测得混合溶液的pH=y,下列推断不正确的是( )
| A、当x=0.2,则混合溶液中y可能大于7或小于7 |
| B、当x=0.2,y=1,则混合溶液中:c(H+)=c(A2-)+c(OH-) |
| C、当x=0.3,y>7,则混合溶液中:c(Na+)>c(A2-)>c(HA-)>c(OH-)>c(H+) |
| D、当x=0.4,则混合溶液中:[c(Na+)+c(H+)]>2c(A2-) |
 X、Y、Z、R为前四周期元素,且原子序数依次增大.常温下X的氢化物XH3溶于水PH>7;Y是地壳里含量最多的金属元素,其单质与酸碱均能反应;Z2有毒,其水溶液有漂白性;R基态原子3d轨道的电子数是4S轨道的电子数的3倍,RZ2溶液呈浅绿色.回答下列问题:
X、Y、Z、R为前四周期元素,且原子序数依次增大.常温下X的氢化物XH3溶于水PH>7;Y是地壳里含量最多的金属元素,其单质与酸碱均能反应;Z2有毒,其水溶液有漂白性;R基态原子3d轨道的电子数是4S轨道的电子数的3倍,RZ2溶液呈浅绿色.回答下列问题: