题目内容
下列离子方程式书写正确的是( )
| A、将铜屑加入含Fe3+溶液中:Fe3++Cu═Fe2++Cu2+ |
| B、NaOH溶液与氧化铝反应:Al2O3+2OH-═2AlO2-+H2O |
| C、NaHCO3溶液中加入氢氧化钠溶液:HCO3-+OH-═CO2↑+H2O |
| D、向Fe(OH)2中加入足量稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电子、电荷不守恒;
B.反应生成偏铝酸钠和水;
C.反应生成碳酸钠和水;
D.发生氧化还原反应生成硝酸铁、NO和水.
B.反应生成偏铝酸钠和水;
C.反应生成碳酸钠和水;
D.发生氧化还原反应生成硝酸铁、NO和水.
解答:
解:A.将铜屑加入含Fe3+溶液中的离子反应为2Fe3++Cu═2Fe2++Cu2+,故A错误;
B.NaOH溶液与氧化铝反应的离子反应为Al2O3+2OH-═2AlO2-+H2O,故B正确;
C.NaHCO3溶液中加入氢氧化钠溶液的离子反应为HCO3-+OH-═CO32-+H2O,故C错误;
D.向Fe(OH)2中加入足量稀硝酸的离子反应为NO3-+3Fe(OH)2+10H+═3Fe3++NO↑+8H2O,故D错误;
故选B.
B.NaOH溶液与氧化铝反应的离子反应为Al2O3+2OH-═2AlO2-+H2O,故B正确;
C.NaHCO3溶液中加入氢氧化钠溶液的离子反应为HCO3-+OH-═CO32-+H2O,故C错误;
D.向Fe(OH)2中加入足量稀硝酸的离子反应为NO3-+3Fe(OH)2+10H+═3Fe3++NO↑+8H2O,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Zn | Cu | CuCl2 |
| B | Zn | Cu | ZnCl2 |
| C | Cu | Zn | CuSO4 |
| D | Cu | Zn | ZnSO4 |
| A、A | B、B | C、C | D、D |
下列溶液中的氯离子浓度与50mL 1mol/L的AlCl3溶液中氯离子浓度相等的是( )
| A、50 mL 1 mol/L的NaCl |
| B、100 mL 3 mol/L的NH4Cl |
| C、75 mL 2 mol/L的KCl |
| D、75 mL 2 mol/L的CaCl2 |
下列物质中只有离子键的是( )
| A、O2 |
| B、NaOH |
| C、H2O |
| D、NaCl |
下列离子方程式中正确的是( )
| A、少量SO2通入NaOH 溶液中:OH-+SO2→HSO3- |
| B、H2S 通入氯水中:S2-+Cl2→S↓+2Cl- |
| C、二氧化氮溶于水:3NO2+H2O=2H++2NO3-+NO↑ |
| D、H2SO4 与Ba(OH)2 溶液反应:H++SO42-+Ba2++OH-→BaSO4↓+H2O |
下列化学用语正确的是( )
A、硫原子的原子结构示意图: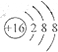 | ||
B、CH4分子的比例模型: | ||
| C、乙烯的结构简式:CH2CH2 | ||
D、原子核内有10个中子的氧原子:
|
下列离子方程式的书写正确的是( )
| A、Cu与AgNO3溶液反应:Cu+Ag+═Cu2++Ag |
| B、Fe与盐酸的反应放出H2:Fe+2H+═Fe2++H2↑ |
| C、大理石与盐酸反应放出CO2气体:CO32-+2H+═CO2↑+H2O |
| D、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ |
瓦斯中甲烷与氧气的体积比为1:2时极易爆炸,则此时甲烷与氧气的质量比为( )
| A、1:1 | B、2:1 |
| C、1:4 | D、4:1 |
 铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成.