题目内容
8.已知2Al+2NaOH+2H2O→2NaAlO2+3H2↑.该反应中有关物理量的描述正确的是(NA表示阿伏伽德罗常数)( )| A. | 每生成0.3molH2,被还原的水分子数目为0.6NA | |
| B. | 当有2.7gAl参加反应时,转移的电子数目为0.3NA | |
| C. | 每生成6.72L的H2,溶液中AlO2-的数目就增加0.2NA | |
| D. | 溶液中每增加0.1mol的AlO2-,Na+的数目就增加0.1NA |
分析 该反应中铝失电子作还原剂,氢元素得电子作氧化剂,只有水作氧化剂,再根据各种微粒之间的关系式计算,注意弱根离子易水解,据此进行解答.
解答 解:该反应中铝失电子作还原剂,氢元素得电子作氧化剂,所以只有水作氧化剂,
A.反应过程为:2Al+6H2O═2Al(OH)3+3H2↑,Al(OH)3+2NaOH═NaAlO2+2H2O,由2Al+6H2O═2Al(OH)3+3H2↑可知,每生成0.3 mol H2,被还原的水分子数目为0.6NA,故A正确;
B.根据方程式知,当有2.7 g Al参加反应时,转移的电子数目=$\frac{2.7g}{27g/mol}$×3×NA=0.3NA,故B正确;
C.没有指出在标准状况下,不能使用标准状况下的气体摩尔体积计算氢气的物质的量,故C错误;
D.偏铝酸钠化学式中Na+和AlO2-的个数之比是1:1,但在溶液中,AlO2-易水解而Na+不水解,导致Na+个数大于AlO2-个数,所以溶液中每增加0.1 mol的AlO2-,Na+的数目增加量大于0.1 NA,故D错误;
故选AB.
点评 本题考查了氧化还原反应的计算、物质的量的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握电子守恒的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
19.下列说法正确的是( )
| A. | 乙烯能使酸性高锰酸钾溶液褪色,发生了加成反应 | |
| B. | 苯可以使溴水褪色,发生了取代反应 | |
| C. | 乙醛在一定条件下与氢气反应生成乙醇,发生了氧化反应 | |
| D. | 苯在一定条件下能与浓硝酸反应得到硝基苯,发生了取代反应 |
3.化工厂经常用浓氨水检验输送氯气的管道是否漏气,其反应为3Cl2+8NH3=N2+6NH4Cl,当有3mol NH4Cl产生时,被氧化的氨气是( )
| A. | 4mol | B. | 1mol | C. | 8mol | D. | 2mol |
12.下列各对物质中,互为同系物的是( )
| A. | CH4、C2H4 | B. | CH4、C2H5OH | C. | C2H6、C3H8 | D. | CH3COOH、C3H6 |
10.下列化学用语正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | CO2的比例模型: | ||
| C. | 醛基的电子式: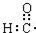 | D. | 含有10个中子的氧原子:188O |
 请完成并配平上列的离子方程式.
请完成并配平上列的离子方程式.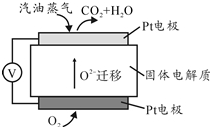 为摆脱对石油的过度依赖,科研人员将煤液化制备汽油,并设计了汽油燃料电池,电池工作原理如图所示:一个电极通入氧气,另一电极通入汽油蒸气,电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O${\;}_{2}^{-}$
为摆脱对石油的过度依赖,科研人员将煤液化制备汽油,并设计了汽油燃料电池,电池工作原理如图所示:一个电极通入氧气,另一电极通入汽油蒸气,电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O${\;}_{2}^{-}$