题目内容
某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:
①向该待测液中加入过量的稀盐酸,有白色沉淀生成.
②过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成.
③过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现.
④另取少量步骤③中的滤液,加入NaOH溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体.
根据实验现象回答:
(1)待测液中一定含有 离子,一定不含有 离子.
(2)还有一种离子无法确定是否存在,检验该离子实验方法的名称是 观察到的现象是 .
①向该待测液中加入过量的稀盐酸,有白色沉淀生成.
②过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成.
③过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现.
④另取少量步骤③中的滤液,加入NaOH溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体.
根据实验现象回答:
(1)待测液中一定含有
(2)还有一种离子无法确定是否存在,检验该离子实验方法的名称是
考点:常见阴离子的检验,常见阳离子的检验
专题:
分析:①加入过量盐酸有白色沉淀生成,说明一定含有银离子;
②在滤液中加入过量的稀硫酸,又有白色沉淀生成说明含有钡离子;
③滴入2滴KSCN溶液,没有明显的现象出现,证明无铁离子;
④加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体,证明含有铵根离子.
②在滤液中加入过量的稀硫酸,又有白色沉淀生成说明含有钡离子;
③滴入2滴KSCN溶液,没有明显的现象出现,证明无铁离子;
④加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体,证明含有铵根离子.
解答:
解:①加入过量盐酸有白色沉淀,说明一定含有Ag+;
②在滤液中加入过量的稀硫酸,又有白色沉淀生成,说明含有Ba2+;
③滴入2滴KSCN溶液,没有明显的现象出现,则证明无Fe3+;
④加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体,证明含有铵根离子;
综上所述:溶液中一定含有Ag+、Ba2+、NH4+;一定不含Fe3+;K+不能确定,需要用焰色反应检验,透过蓝色钴玻璃可以观察到紫色火焰,
故答案为:(1)Ag+、Ba2+、NH4+;Fe3+;(2)焰色反应;用铂丝沾取溶液在酒精灯上灼烧并透过蓝色钴玻璃观察火焰颜色.
②在滤液中加入过量的稀硫酸,又有白色沉淀生成,说明含有Ba2+;
③滴入2滴KSCN溶液,没有明显的现象出现,则证明无Fe3+;
④加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体,证明含有铵根离子;
综上所述:溶液中一定含有Ag+、Ba2+、NH4+;一定不含Fe3+;K+不能确定,需要用焰色反应检验,透过蓝色钴玻璃可以观察到紫色火焰,
故答案为:(1)Ag+、Ba2+、NH4+;Fe3+;(2)焰色反应;用铂丝沾取溶液在酒精灯上灼烧并透过蓝色钴玻璃观察火焰颜色.
点评:本题考查了常见离子的检验,题目难度中等,注意掌握常见离子的性质及检验方法,明确焰色反应操作方法,特别是检验钾离子的方法,观察焰色反应的火焰时需要通过蓝色钴玻璃观察.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列变化必须加入氧化剂才能实现的是( )
| A、CuO→Cu |
| B、Fe→FeCl2 |
| C、HNO3→NO2 |
| D、CaCO3→CO2 |
欲使0.lmol/L的Na2CO3溶液中c(Na+)接近2c(CO32-),应采取的措施是( )
| A、适当加热 |
| B、适量加NaOH. |
| C、适量加盐酸 |
| D、适量加KOH |
据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源是( )
| A、太阳能 | B、石油 | C、水煤气 | D、煤 |
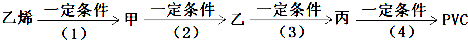
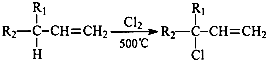
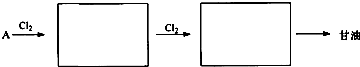

 基团的同分异构体有
基团的同分异构体有 化学是一门以实验为基础的科学.
化学是一门以实验为基础的科学.