题目内容
阿波罗宇宙飞船使用的是氢氧燃料电池,其电极反应为:2H2+4OH-→4H2O+4e-,2H2O+O2+4e-→4OH-.在负极反应的物质是 ,负极发生的是 (填氧化或还原)反应,电池反应是 ,若用稀硫酸作电解质,负极反应方程式 ,正极反应方程式是 .
考点:化学电源新型电池
专题:电化学专题
分析:氢氧燃料碱性电池中,负极上燃料失电子发生氧化反应,正极上氧化剂得电子发生还原反应,在得失电子相同的条件下将正负极电极反应式相加即得电池反应式;当稀硫酸为电解质溶液时,负极上氢气失电子生成氢离子,正极上氧气得电子和氢离子反应生成水.
解答:
解:氢氧燃料碱性电池中,负极上燃料失电子发生氧化反应,所以在负极反应的物质是H2,正极上氧化剂得电子发生还原反应,在得失电子相同的条件下将正负极电极反应式相加即得电池反应式,所以电池反应式为2H2+O2=2H2O;当稀硫酸为电解质溶液时,负极上氢气失电子生成氢离子,正极上氧气得电子和氢离子反应生成水,则负极、正极反应式分别为2H2-4e-═4H+、O2+4H++4e-═2H2O;
故答案为:H2;氧化;2H2+O2=2H2O;2H2-4e-═4H+;O2+4H++4e-═2H2O.
故答案为:H2;氧化;2H2+O2=2H2O;2H2-4e-═4H+;O2+4H++4e-═2H2O.
点评:本题考查燃料电池,明确燃料电池中正负极上发生的反应是解本题关键,会正确书写电极反应式,注意电解反应式与电解质溶液酸碱性有关.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在蒸馏实验中,下列操作叙述不正确的是( )
A、在蒸馏烧瓶中盛约
| ||
| B、将温度计水银球与支管口保持水平 | ||
| C、冷水从冷凝管上口入,下口出 | ||
| D、收集蒸馏水时,应弃去开始馏出的部分 |
分子量为43的烃基取代甲苯苯环上的一个氢原子,所得芳香烃的数目为( )
| A、3 | B、4 | C、5 | D、6 |
下列说法正确的是( )
| A、原电池是把电能转化为化学能的装置 |
| B、原电池中电子流出的一极是正极发生氧化反应 |
| C、原电池的两极发生的反应均为氧化还原反应 |
| D、形成原电池后,原电池中的阳离子向正极移动 |
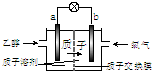 一种新型的乙醇电池(DEFC)是用磺酸类质子溶剂作电解质,在200℃左右时供电(如图所示),比甲醇电池效率高出32倍,且安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O.则下列说法正确的是( )
一种新型的乙醇电池(DEFC)是用磺酸类质子溶剂作电解质,在200℃左右时供电(如图所示),比甲醇电池效率高出32倍,且安全.电池总反应为:C2H5OH+3O2═2CO2+3H2O.则下列说法正确的是( )| A、a极为电池的正极 |
| B、电池正极的电极反应:4H++O2+4e-=2H2O |
| C、电池工作时电子由b极沿导线经灯泡再到a极 |
| D、设每个电子所带电量为q库仑,则1mol乙醇被氧化产生6q×6.02×1023库仑的电量 |
下列离子方程式不正确的是( )
| A、银氨溶液中加入足量盐酸产生沉淀:[Ag(NH3)2]++OH-+3H++Cl-=AgCl↓+2NH4++H2O |
| B、在亚硫酸钡沉淀中加入稀硝酸后,沉淀不溶解:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O |
| C、碳酸钠溶液中通入少量SO2:2CO32-+SO2+H2O=2HCO3-+SO32- |
| D、氧化铁可溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O |
重水D2O的离子积为1.6×10-15,可以用pH一样的定义来规定pD=-lgc(D+),以下关于pD的叙述正确的是( )
| A、中性溶液中pD=7 |
| B、在1LD2O的溶液中溶解0.01mol NaOD(设溶液的体积为1L),其中pD=12 |
| C、在1L D2O中溶解 0.01mol DCl (设溶液的体积为1L),其中pD=2 |
| D、在100 mL 0.25mol/L的DCl重水溶液中加入100 mL 0.2 mol/L的 NaOD的重水溶液,其中pD=1 |
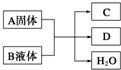 A、B、C、D都是中学常见的物质,在一定的条件下有如图所示的转化关系(未注明反应条件),请回答下列问题:
A、B、C、D都是中学常见的物质,在一定的条件下有如图所示的转化关系(未注明反应条件),请回答下列问题: