��Ŀ����
ij���������Լ�ƿ��ǩ�ϵIJ�����Ϣ����:
���� ����ʽ:HCl ��Է�������:36.5 �ܶ�Լ1.18 g��mL-1 HCl����������:36.5% |
��1������������ʵ���Ũ��= ,����ȡ��100ml������HCl�����ʵ���Ϊ ������Cl-������Ϊ ��
��2��ȡ������50 mL��ˮϡ�͵�500 mL,��ϡ�ͺ���Һ��C(HCl)= ,����ȡ��10ml����Ũ��Ϊ ��
��3��ȡϡ�ͺ������������п������,������ ��
ú̿���ҹ�����Ҫ��Դ֮һ����֮�����Ķ�������(SO2)��������Ⱦ�����Ϊͻ����Ŀǰ�ҹ����õĿ��Ʒ����ǵ糧�����������������ԭ�������ü����������ղ��̶����ԵĶ���������Ҫ���������ַ�����
I���Ƽ�ѭ������������
(1)�˷�������Na2SO3��Һ���ѳ������е�SO2��Na2SO3����NaOH��Һ����SO2�Ƶã��÷�Ӧ�����ӷ���ʽ�� ��
(2)NaOH��Һ����SO�Ĺ����У�pH��n(SO32-)��n(HSO3-)�仯��ϵ���±���
n(SO32-)��n(HSO3-) | 91��9 | 1��1 | 9��91 |
pH | 8.2 | 7.2 | 6.2 |
�����ϱ��жϣ�NaHSO3��Һ�� �ԣ��û�ѧƽ��ԭ�����ͣ� ��
�ڵ���Һ������ʱ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ)�� ��
a��c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
b��c(Na+)��c(HSO3-)��c(SO32-)��c(H-)=c(OH-)
c��c(Na+)=2c(SO32-)+c(HSO3-)
II��ʯ��ʯ����
�˷�����ʯ��ʯΪԭ��ͨ��ϵ�з�Ӧ����Ԫ����CaSO4����ʽ�̶����Ӷ�����SO2���ŷš�����ú̿ȼ�չ����в�����CO�ֻ���CaSO4������ѧ��Ӧ����������Ч�ʡ���ط�Ӧ���Ȼ�ѧ����ʽ���£�
CaSO4(s)+CO(g)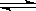 CaO(s)+SO2(g)+CO2(g)��H=218.4kJ��mol-1(��Ӧ��)
CaO(s)+SO2(g)+CO2(g)��H=218.4kJ��mol-1(��Ӧ��)
CaSO4(s)+4CO(g)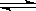 CaS(s)+4CO2(g)��H2=-175.6kJ��mol-1(��Ӧ��)
CaS(s)+4CO2(g)��H2=-175.6kJ��mol-1(��Ӧ��)
��ش��������⣺
(1)��Ϸ�Ӧ��д��CaSO4(s)��CaS(s) ���Ȼ�ѧ��Ӧ����ʽ ��
(2)�����������ķ�Ӧ����ʾƽ�ⳣ�� Kpʱ���������(B)��ƽ��ѹǿp(B)������������ʵ���Ũ��c(B)����Ӧ���Kp= (�ñ���ʽ��ʾ)��
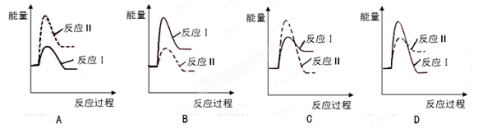
(3)����ij�¶��£���Ӧ�������(v1)С�ڷ�Ӧ�������(v2)�������з�Ӧ���������仯ʾ��ͼ��ȷ���� ��
(4)ͼ1Ϊʵ���ò�ͬ�¶��·�Ӧ��ϵ��CO��ʼ����ٷ�����ƽ��ʱ���������CaS�����ٷ����Ĺ�ϵ���ߡ��÷�Ӧ��ϵ�в�����SO2�������Ĵ�ʩ�� ��
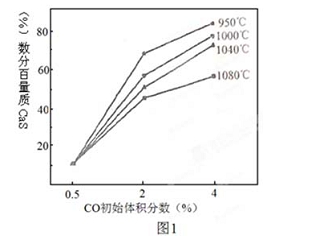
A����÷�Ӧ��ϵ��Ͷ����ʯ��
B���ں��ʵ��¶������ڿ��ƽϵ͵ķ�Ӧ�¶�
C������CO�ij�ʼ����ٷ���
D����߷�Ӧ��ϵ���¶�


 xC(��)+3D(��)����Ӧƽ��ı�Ӱ��ƽ���һ������������A��Ũ�ȱ仯����ͼ��ʾ�������й�˵����ȷ����
xC(��)+3D(��)����Ӧƽ��ı�Ӱ��ƽ���һ������������A��Ũ�ȱ仯����ͼ��ʾ�������й�˵����ȷ����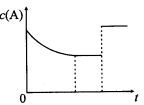
 ��100 mL 1 mol��L-1Na2CO3��Һ����������������0.1 NA
��100 mL 1 mol��L-1Na2CO3��Һ����������������0.1 NA �бȽ���ȷ
�бȽ���ȷ