题目内容
用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、标准状态下,22.4LC4H6中含有碳碳叁键数一定为NA |
| B、含1molFeCl3的饱和溶液滴入沸水中得到氢氧化铁胶体粒子数目为NA |
| C、在标准状况下,22.4L辛烷中所含分子数为NA |
| D、106 g Na2CO3固体中的阴离子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.C4H6分子可能为1,3-丁二烯,其分子中不一定含有碳碳三键;
B.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算胶体中含有的氢氧化铁胶粒数;
C.标准状况下,辛烷的状态为液体,不能使用标况下的气体摩尔体积计算其物质的量;
D.106g碳酸钠的物质的量为1mol,1mol碳酸钠中含有1mol碳酸根离子.
B.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算胶体中含有的氢氧化铁胶粒数;
C.标准状况下,辛烷的状态为液体,不能使用标况下的气体摩尔体积计算其物质的量;
D.106g碳酸钠的物质的量为1mol,1mol碳酸钠中含有1mol碳酸根离子.
解答:
解:A.C4H6不一定为炔烃,可能为1,3-丁二烯,其分子中不一定含有碳碳三键,故A错误;
B.氢氧化铁胶体粒子为氢氧化铁的聚集体,无法计算胶体中含有胶粒数,故B错误;
C.标况下,辛烷不是气体,不能使用标况下的气体摩尔体积计算22.4L辛烷的物质的量,故C错误;
D.106g碳酸钠的物质的量为:
=1mol,含有1mol碳酸根离子,含有的阴离子数为NA,故D正确;
故选D.
B.氢氧化铁胶体粒子为氢氧化铁的聚集体,无法计算胶体中含有胶粒数,故B错误;
C.标况下,辛烷不是气体,不能使用标况下的气体摩尔体积计算22.4L辛烷的物质的量,故C错误;
D.106g碳酸钠的物质的量为:
| 106g |
| 106g/mol |
故选D.
点评:本题考查阿伏加德罗常数的判断,题目难度中等,注意明确氢氧化铁胶粒为氢氧化铁的聚集体,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项A为易错点,注意C4H6分子不一定为炔烃.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案
相关题目
2001年诺贝尔化学奖授予在“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家.下列分子含有手性碳原子的是( )
| A、CHFBr2 |
| B、CH3CH2OH |
C、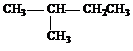 |
D、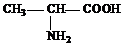 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、100mL 0.1mol?L-1的稀硫酸中含有SO42-的个数为0.1NA |
| B、每有1mol Fe参加氧化还原反应失去电子数目均为2NA |
| C、标准状况下,22.4L水所含水分子数为NA |
| D、标准状况下,足量锌与稀硫酸反应每生成1mol氢气转移电子数为2NA |
下列有关金属铝及其化合物的叙述正确的是( )
| A、铝片在空气能与氧气剧烈燃烧并放出大量的热 |
| B、工业上用电解氯化铝生产铝 |
| C、氢氧化铝在溶液中只能电离出铝离子 |
| D、硫酸铝钾溶液中滴入足量的氢氧化钡溶液,则得到的沉淀只有硫酸钡 |
下列各组试剂中,只用试管和胶头滴管,不用其他试剂就可以鉴别的是( )
| A、NaOH(aq)和Al2(SO4)3(aq) |
| B、稀盐酸和AgNO3(aq) |
| C、CaCl2(aq)和Na2CO3(aq) |
| D、Ba(OH)2(aq)和Na2SO4(aq) |