题目内容
16.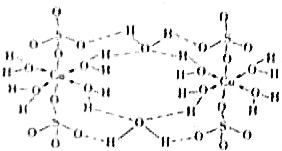 下列说法正确的是( )
下列说法正确的是( )| A. | 在如图结构示意图中,所有氧原子都采用sp3杂化 | |
| B. | 在如图结构示意图中,存在配位键、共价键和离子键 | |
| C. | 胆矾是分子晶体,分子间存在氢键 | |
| D. | 胆矾中的水在不同温度下会分步失去 |
分析 A.硫酸根离子中羟基氧是sp3杂化,非羟基氧不是中心原子原子,不参与杂化杂化;
B.在上述结构示意图中,存在O→Cu配位键,H-O、S-O共价键,配离子与硫酸根之间形成离子键;
C.胆矾是五水硫酸铜,胆矾是由水合铜离子及硫酸根离子构成的,属于离子晶体;
D.由于胆矾晶体中水两类,一类是形成配体的水分子,一类是形成氢键的水分子.
解答 解:A.水中O原子为sp3杂化,硫酸根离子中羟基氧是sp3杂化,非羟基氧不是中心原子原子,不参与杂化杂化,故A错误;
B.在上述结构示意图中,存在O→Cu配位键,H-O、S-O共价键,配离子与硫酸根之间形成离子键,故B正确;
C.胆矾是五水硫酸铜,胆矾是由水合铜离子及硫酸根离子构成的,属于离子晶体,故C错误;
D.由于胆矾晶体中水两类,一类是形成配体的水分子,一类是形成氢键的水分子,结构上有着不同,胆矾中的水在不同温度下会分步失去,故D正确,
故选BD.
点评 本题考查配合物、化学键、杂化方式判断等,属于易错题目,侧重考查学生分析能力,难度中等.

练习册系列答案
相关题目
4.下列物质碱性最强的是( )
| A. | LiOH | B. | KOH | C. | RbOH | D. | NaOH |
1.恒温下,在一密闭容器中,N2(g)+3H2(g)?2NH3(g)达到平衡后,测得c(H2)=2mol•L-1,N2的体积分数为20%,下列有关说法中正确的是( )
| A. | 将容器容积压缩一半,平衡向右移动,达到新平衡时c(H2)<2mol•L-1 | |
| B. | 向容器中加入0.1molN2,平衡向右移动,达到新平衡时N2的体积分数小于20% | |
| C. | 若达到新平衡时c(H2)=2.5mol•L-1,则改变的条件可能是降温或加压 | |
| D. | 若改变条件后,H2的百分含量增大,则平衡一定向逆反应方向移动 |
4.下列说法错误的是( )
| A. | 金属甲比金属乙容易失去电子,则甲比乙金属性强 | |
| B. | NaHCO3与NaOH反应有CO2生成 | |
| C. | 稀硝酸能将亚铁离子氧化为铁离子 | |
| D. | Na2CO3不能用于治疗胃酸过多 |
1.短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最高的元素,Y是同周期中原子半径最大的元素,Z的最高氧化物的水化物能分别与Y和W的最高氧化的水化物反应生成盐和水,X与W同主族.下列说法不正确的是( )
| A. | X与Y只能形成一种化合物 | |
| B. | 原子半径:r(W)<r(Z)<r(Y) | |
| C. | X的简单气态氢化物的热稳定性比W的强 | |
| D. | Z的最高价氧化物对应的水化物具有两性 |
2.某晶体中含有极性键,关于该晶体的说法错误的是( )
| A. | 不可能有很高的熔沸点 | B. | 不可能是金属晶体 | ||
| C. | 可能是有机物 | D. | 可能是离子晶体 |
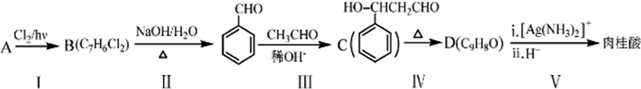

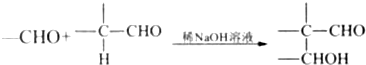
 .
. .肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是
.肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是 .
.